
【题目】根据化学原理的相关知识填空。
⑴常温时,![]() 的水溶液呈酸性,原因是
的水溶液呈酸性,原因是![]() 用离子方程式表示
用离子方程式表示![]() :___________,将
:___________,将![]() 溶液蒸干,灼烧,最后得到的固体产物主要是__________
溶液蒸干,灼烧,最后得到的固体产物主要是__________![]() 填化学式
填化学式![]() 。
。
⑵向![]() 溶液滴加石蕊溶液后变红,则
溶液滴加石蕊溶液后变红,则![]() 的电离程度______其水解程度
的电离程度______其水解程度![]() 填“
填“![]() ”或“
”或“![]() ”或“
”或“![]() ”
”![]() 。该物质能_______
。该物质能_______![]() 填“促进”或“抑制”
填“促进”或“抑制”![]() 水的电离。
水的电离。
⑶若想除去![]() 溶液中混有
溶液中混有![]() 杂质,则往往加入试剂 ________。
杂质,则往往加入试剂 ________。
![]()
![]()
![]()
![]()
⑷泡沫灭火器的灭火原理为___________![]() 用离子方程式解释
用离子方程式解释![]()
⑸在苏打溶液中存在的电荷守恒式为__________;质子守恒式为__________
⑹常温下,物质的量浓度相同的下列溶液:![]()
![]()
![]()
![]()
![]() 溶液中
溶液中![]() 从大到小排列顺序为________
从大到小排列顺序为________![]() 填序号
填序号![]() 。
。
⑺现有a.醋酸、b.盐酸、c.硫酸三种溶液,根据要求答题。
![]() 若它们物质的量浓度相等,它们的pH由大到小的关系为_______(用abc表示,下同)。
若它们物质的量浓度相等,它们的pH由大到小的关系为_______(用abc表示,下同)。
![]() 若它们的pH相等,它们物质的量浓度由大到小的关系为_____。
若它们的pH相等,它们物质的量浓度由大到小的关系为_____。
![]() 若它们的pH相等,均加水稀释100倍后,其pH由大到小的关系为________。
若它们的pH相等,均加水稀释100倍后,其pH由大到小的关系为________。
【答案】![]()
![]()
![]() 抑制
抑制 ![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
【解析】
⑴常温时,![]() 的水溶液水解显酸性,HCl易挥发,因此
的水溶液水解显酸性,HCl易挥发,因此![]() 溶液蒸干,灼烧,得到最后的固体产物。
溶液蒸干,灼烧,得到最后的固体产物。
⑵向![]() 溶液滴加石蕊溶液后变红,显酸性。
溶液滴加石蕊溶液后变红,显酸性。
⑶若想除去![]() 溶液中混有
溶液中混有![]() 杂质,利用铁离子水解,加对应的被提纯物质的难溶于水的氧化物或碳酸物。
杂质,利用铁离子水解,加对应的被提纯物质的难溶于水的氧化物或碳酸物。
⑷泡沫灭火器的灭火原理硫酸铝和碳酸氢钠反应。
⑸根据苏打溶液中存在的电荷守恒式,质子守恒式写出。
⑹常温下,物质的量浓度相同的各种溶液中铵根离子水解与其它离子之间的关联。
⑺利用醋酸部分电离,盐酸、硫酸全部电离思想以及一元强酸和一元弱酸的比较来解题。
⑴![]() 为强酸弱碱盐,
为强酸弱碱盐,![]() 水解溶液呈酸性,离子方程式为:
水解溶液呈酸性,离子方程式为:![]() ;
;![]() 溶液蒸干,水解生成的氯化氢挥发,水解正向进行得到水解产物氢氧化铝,灼烧得到氧化铝(Al2O3);故答案为:
溶液蒸干,水解生成的氯化氢挥发,水解正向进行得到水解产物氢氧化铝,灼烧得到氧化铝(Al2O3);故答案为:![]() ;
;![]() 。
。
⑵向![]() 溶液滴加石蕊溶液后变红则溶液显酸性,则
溶液滴加石蕊溶液后变红则溶液显酸性,则![]() 的电离程度大于其水解程度;
的电离程度大于其水解程度;![]() 电离的氢离子抑制水的电离;故答案为:
电离的氢离子抑制水的电离;故答案为:![]() ;抑制。
;抑制。
⑶![]() 会与
会与![]() 反应不可用;
反应不可用;![]() 会与
会与![]() 反应不可用;
反应不可用;![]() 发生水解
发生水解![]() ,CuO消耗水解生成的
,CuO消耗水解生成的![]() ,使平衡正向移动,可促进水解又不引入新的杂质,过量也可以一起过滤除去,故可除杂;
,使平衡正向移动,可促进水解又不引入新的杂质,过量也可以一起过滤除去,故可除杂;![]() 发生水解
发生水解![]() ,
,![]() 消耗水解生成的
消耗水解生成的![]() ,使平衡正向移动,可促进水解又不引入新的杂质,过量也可以一起过滤除去,故可除杂;故答案为:
,使平衡正向移动,可促进水解又不引入新的杂质,过量也可以一起过滤除去,故可除杂;故答案为:![]() 。
。
⑷泡沫灭火器的灭火原理为硫酸铝和碳酸氢钠反应生成氢氧化铝沉淀、硫酸钠和二氧化碳,离子方程式为:![]() ;故答案为:
;故答案为:![]() 。
。
⑸苏打溶液含有的阳离子有钠离子、氢离子,阴离子有氢氧根离子、碳酸根离子和碳酸氢根离子,故含有电荷守恒![]() ;水中电离出
;水中电离出![]() 等于水电离出的
等于水电离出的![]() ,溶液中
,溶液中![]() 中的H和
中的H和![]() 中的H均来自水电离的
中的H均来自水电离的![]() ,故苏打溶液中质子守恒式为
,故苏打溶液中质子守恒式为![]() ;故答案为:
;故答案为:![]() ;
;![]() 。
。
⑹![]() 和
和![]() 的铵离子浓度大,
的铵离子浓度大,![]() 溶液中的
溶液中的![]() 会减弱
会减弱![]() 的水解,故
的水解,故![]() 溶液中
溶液中![]() 大于
大于![]() ;
;![]() 中电离出的
中电离出的![]() 会抑制
会抑制![]() 的水解,故
的水解,故![]() 溶液中
溶液中![]() 大于
大于![]() 和
和![]() ;
;![]() 中
中![]() 溶液中
溶液中![]() 与
与![]() 发生双水解,故
发生双水解,故![]() 溶液中
溶液中![]() 小于
小于![]() ;故答案为:
;故答案为:![]() 。
。
⑺![]() 盐酸、硫酸都为强酸,相同物质的量浓度下,为二元强酸的硫酸
盐酸、硫酸都为强酸,相同物质的量浓度下,为二元强酸的硫酸![]() 电离的
电离的![]() 比盐酸
比盐酸![]() 电离的
电离的![]() 多,醋酸为一元弱酸,电离的
多,醋酸为一元弱酸,电离的![]() 最少,故
最少,故![]() 的由大到小是cba,而
的由大到小是cba,而![]() 越多,pH越小,故pH由大到小为abc;
越多,pH越小,故pH由大到小为abc;![]() 若它们的pH相等,即电离的
若它们的pH相等,即电离的![]() 相等,与
相等,与![]() 中逆推,可知它们物质的量浓度由大到小为abc;
中逆推,可知它们物质的量浓度由大到小为abc;![]() 若它们的pH相等,强酸的
若它们的pH相等,强酸的![]() 全部电离,稀释同等倍数的pH增长相同,但弱酸越稀,越促进其电离,故醋酸的pH增大值没有强酸快,故pH由大到小的关系为
全部电离,稀释同等倍数的pH增长相同,但弱酸越稀,越促进其电离,故醋酸的pH增大值没有强酸快,故pH由大到小的关系为![]() ;故答案为:abc;abc;
;故答案为:abc;abc;![]() 。
。


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
【题目】T ℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示。
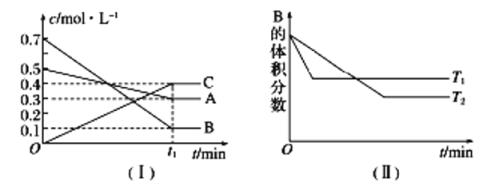
根据以上条件,回答下列问题:
(1)A与B反应生成C的化学方程式为________,正反应为_____(填“吸热”或“放热”)反应。
(2)t1 min后,改变下列某一条件,能使平衡向逆反应方向移动的有______(填字母序号)。
A.保持其他条件不变,增大压强
B.保持容器总体积不变,通入少量稀有气体
C.保持其他条件不变,升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实能用勒夏特列原理解释的是( )
A.工业上N2与H2合成NH3,往往需要使用催化剂
B.密闭容器中2molCO与1molH2O(g)充分反应达平衡后,增大压强CO的反应速率加快
C.SO2与O2催化氧化成SO3是一个放热过程,450℃左右的温度比室温更有利于SO3生成
D.向1.50mol/L的硝酸铵溶液中加入少量氨水至中性,水的电离程度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项内容,排列顺序正确是( )
①固体的热稳定性:Na2CO3>CaCO3>NaHCO3
②常见离子的还原性排序:S2->I->Fe2+
③微粒半径:K+>S2->F-
④给出质子的能力:CH3COOH>C2H3OH>H2O
⑤氢化物的沸点:H2Se>H2S>H2O
A.①③B.②④C.①②D.③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如图所示实验,探究反应中的能量变化。

下列判断正确的是( )
A.由实验可知,(a)、(b)、(c)所涉及的反应都是放热反应
B.将实验(a)中的铝片更换为等质量的铝粉后释放出的热量有所增加
C.实验(c)中将环形玻璃搅拌棒改为铁质搅拌棒对实验结果没有影响
D.若用NaOH固体测定中和热,则测定中和热的数值偏高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.将一定体积醋酸溶液加水到原来体积的m倍,则pH增大m
B.在NaHCO3溶液中,c(Na+)=c(HCO3-)+c(H2CO3)
C.25℃,pH=8的NaOH溶液和pH=8的氨水中,由水电离出的c(OH-)不相等
D.25℃,pH=13的Ba(OH)2溶液和pH=1的盐酸中均存在:c(H+)·c(OH-)=1×10-14
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸即乙二酸,是一种有机二元酸,在工业上有重要的作用。已知![]() 的电离常数:
的电离常数:![]() ,
,![]() ;
;![]() 电离常数:
电离常数:![]()
⑴![]() 溶液的pH______
溶液的pH______![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() 。
。
⑵用惰性电极电解饱和草酸溶液可制得乙醛酸![]() 。阴极的电极反应式为_____。
。阴极的电极反应式为_____。
⑶草酸钠是一种重要的还原剂。合成草酸钠的操作如下:草酸![]()
![]()
![]() 草酸钠晶体
草酸钠晶体
![]() 酒精的作用是________________。
酒精的作用是________________。
![]() 当草酸与碳酸钠的物质的量按2:1充分混合后,溶液中
当草酸与碳酸钠的物质的量按2:1充分混合后,溶液中![]() 。请将该溶液中离子浓度按由大到小的顺序排列______。
。请将该溶液中离子浓度按由大到小的顺序排列______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五倍子是一种常见的中草药,其有效成分为X。一定条件下X可分别转化为Y、Z,如下所示。
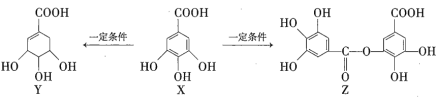
下列说法错误的是( )
A.![]() 最多能与
最多能与![]() 发生取代反应
发生取代反应
B.等物质的量的Z分别与Na和![]() 恰好反应时,消耗Na和
恰好反应时,消耗Na和![]() 的物质的量之比为6∶1
的物质的量之比为6∶1
C.一定条件下,Y能发生加成反应、取代反应、消去反应和氧化反应
D.![]() 最多能与
最多能与![]() 发生反应
发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。已知:2KMnO4+16HCl―→2KCl+5Cl2↑+2MnCl2+8H2O
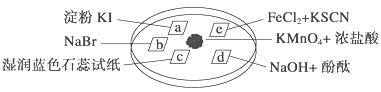
对实验现象的“解释或结论”正确的是 ( )
选项 | 实验现象 | 解释或结论 |
A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
C | d处立即褪色 | 氯气与水生成了漂白性物质 |
D | e处变红色 | 还原性:Fe2+>Cl- |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com