
下列曲线图(纵坐标为沉淀的量,横坐标为加入物的量)与对应选项不正确的是( )

|
| A. | 向1L浓度均为0.1mol/L的Ba(OH)2、NaAlO2混合液中加入0.1 mol/L稀H2SO4溶液 |
|
| B. | 向含有0.1 mol/L AlCl3和0.3mol/L NH4Cl的1L混合液中加入0.1mol/L NaOH溶液 |
|
| C. | 向烧碱溶液中滴加明矾溶液 |
|
| D. | 向Ca(OH)2溶液中逐渐通入二氧化碳 |
| 镁、铝的重要化合物. | |
| 专题: | 图示题. |
| 分析: | A、Ba(OH)2、NaAlO2混合液中加入稀H2SO4溶液,酸碱中和反应先发生,且生成硫酸钡沉淀,然后是硫酸和NaAlO2发生反应的过程; B、AlCl3和 NH4Cl的1L混合液中加入NaOH溶液,先出现白色沉淀氢氧化铝,然后是铵根离子和氢氧根离子之间反应生成一水合氨,最后是氢氧化铝溶解的过程; C、向氢氧化钠中加明矾,开始阶段碱过量,不会出现沉淀,然后是铝离子和偏铝酸盐生成氢氧化铝沉淀的过程; D、Ca(OH)2溶液中逐渐通入二氧化碳,开始会出现白色沉淀,然后沉淀逐渐消失. |
| 解答: | 解:A、Ba(OH)2、NaAlO2混合液中加入稀H2SO4溶液,酸碱中和反应先发生,且生成硫酸钡沉淀,所以反应开始就有沉淀生成,然后是硫酸和NaAlO2发生反应的过程,当加入2.5L硫酸,沉淀氢氧化铝全部溶解,故A错误; B、AlCl3和 NH4Cl的1L混合液中加入NaOH溶液,先出现白色沉淀氢氧化铝,然后是铵根离子和氢氧根离子之间反应生成一水合氨,最后是氢氧化铝溶解的过程,消耗NaOH的量之比是3:3:1,故B正确; C、向氢氧化钠中加明矾,开始阶段碱过量,不会出现沉淀,然后是铝离子和偏铝酸盐生成氢氧化铝沉淀的过程,故C正确; D、Ca(OH)2溶液中逐渐通入二氧化碳,开始会出现白色沉淀,然后沉淀逐渐消失,两个过程消耗的二氧化碳的量相等,故D正确. 故选A. |
| 点评: | 本题考查学生物质的性质以及化学反应发生的先后知识,结合图象来考查,增加了题目的难度. |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列有关元素的性质及其递变规律正确的是
A.ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物
B.第二周期元素从左到右,最高正价从+1递增到+7
C.同主族元素的简单阴离子还原性从上到下依次减弱
D.同周期金属元素的化合价越高,其原子失电子能力越强
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究小组为了探究一种无机矿物盐X(仅含四种元素)的组成和性质,设计并完成了如下实验:

另取10.80 g X在惰性气流中加热至完全分解,得到6.40 g固体1。
请回答如下问题:
(1)画出白色沉淀1中金属元素的原子结构示意图________,写出气体甲的电子式________。
(2)X的化学式是________,在惰性气流中加热X至完全分解的化学反应方程式为____________________。
(3)白色沉淀2在空气中变成红褐色沉淀的原因是____________________(用化学反应方程式表示)。
(4)一定条件下,气体甲与固体1中的某种成分可能发生氧化还原反应,写出一个可能的化学反应方程式____________________,并设计实验方案验证该反应的产物____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
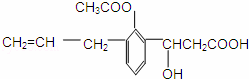
有机物的结构简式如图所示,则此有机物可发生的反应类型有( )
①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦中和.
|
| A. | ①②③⑤⑥ | B. | ①②③④⑤⑥⑦ | C. | ②③④⑤⑥ | D. | ②③④⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下图海水综合利用的工业流程图,判断下列说法正确的是( )

已知:MgCl2•6H2O受热生成Mg(OH)Cl和HCl气体等.
|
| A. | 氯碱工业中电解饱和食盐水是一个将化学能转化为电能的过程 |
|
| B. | 在过程③中将MgCl2•6H2O灼烧即可制得无水MgCl2 |
|
| C. | 在过程④、⑥反应中每氧化0.2 mol Br﹣ 需消耗0.1mol Cl2 |
|
| D. | 过程⑤在生产中无需解决其对金属设备的腐蚀问题 |
查看答案和解析>>
科目:高中化学 来源: 题型:
神舟十号飞船是中国“神舟”号系列飞船之一,它是中国第五艘搭载太空人的飞船.神舟十号飞船发射成功后,将与2011年发射升空的天宫一号目标飞行器进行交会对接,开展相关空间科学试验.火箭推进器是成功发射的重要因素,事实上,推进器的发展经历了一个漫长的过程.
(1)20世纪前,黑火药是世界上唯一的火箭推进剂,黑火药是由硝酸钾、硫磺、木炭组成,黑火药爆炸的化学方程式为:S+2KNO3+3C═K2S+N2↑+3CO2.
(I)K2S的电子式为 ,C02的结构式为 .
②已知S和氯水反应会生成两种强酸,其离子方程式为
③取黑火药爆炸后的残留固体,加水溶解过滤,得到滤液.写出检验此溶液中是否含有K+的实验操作方法.
(2)20世纪60年代,火箭使用的是液体推进剂,常用的氧化剂有四氧化二氮、液氧等,可燃物有麟(N2H4)、液氢等.
①肼(N2H4)溶于水显碱性,其原理与氨相似,但其碱性不如氨强,写出其溶于水呈碱性的离子方程式:
②一种与N2H4电子数相等的绿色氧化剂,能将油画表面黑色的PbS氧化成白色的PbSO4,使油画变白、翻新,化学方程式为: .
(3)以上的火箭推进剂一般含有氮元素,含氮化合物种类丰富.有一含氮化合物,具有很强的爆炸性,86g该化合物爆炸分解会生成标况下N2 67.2L和另一种气体单质H2.写出其爆炸的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
乙醇、乙二醇、丙三醇分别与足量的金属钠作用,产生等量的氢气,则三种醇的物质的量之比为( )
A.6∶3∶2 B.1∶2∶3 C.3∶2∶1 D.4∶3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
无色的混合气体甲中可能含NO、CO2、NO2、NH3、N2中的几种。将100 mL气体甲经过下图实验处理,结果得到酸性溶液,而几乎无气体剩余,则气体甲的组成可能为( )
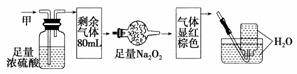
A.NH3、NO2、N2 B.NH3、NO、CO2
C.NH3、NO2、CO2 D.NO、CO2、N2
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物A是农药生产中的一种中间体,其结构简式如图,下列叙述中正确的是( )
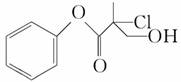
A.有机物A属于芳香烃
B.有机物A可以和Br2的CCl4溶液发生加成反应
C.有机物A和浓硫酸混合加热,可发生消去反应
D.1 mol A和足量的NaOH溶液反应,最多可以消耗3 mol NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com