
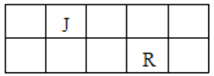
【题目】J、L、M、R、T是原子序数依次增大的短周期元素,J、R在周期表中的相对位置如右表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素。
(1)M的离子结构示意图为_______________;元素T在周期表中位于第_________族。
(2)J和氢组成的化合物分子有6个原子,其结构简式为______________。
(3)M和T形成的化合物在潮湿的空气中冒白色烟雾,反应的化学方程式为_____________________。
(4)L的最简单气态氢化物甲的水溶液显碱性。
在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为______________________________________。
(5)由J、R形成的液态化合物JR2 0.2 mol在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215 kJ。该反应的热化学方程式为______________________________________________。
【答案】 ![]() ⅦA CH2=CH2 AlCl3+3H2O=Al(OH)3↓+3HCl↑ 2NH3·H2O+3H2O2=N2↑+8H2O或2NH3+3H2O2=N2↑+6H2O 1/5 CS2(l)+3/5 O2(g)=1/5 CO2(g)+2/5 SO2(g) △H=-215 kJ·mol-1或CS2(l)+3 O2(g)= CO2(g)+2 SO2(g) △H=-1075 kJ·mol-1
ⅦA CH2=CH2 AlCl3+3H2O=Al(OH)3↓+3HCl↑ 2NH3·H2O+3H2O2=N2↑+8H2O或2NH3+3H2O2=N2↑+6H2O 1/5 CS2(l)+3/5 O2(g)=1/5 CO2(g)+2/5 SO2(g) △H=-215 kJ·mol-1或CS2(l)+3 O2(g)= CO2(g)+2 SO2(g) △H=-1075 kJ·mol-1
【解析】依题意可得J为碳元素,M为铝元素,R为硫元素,T为氯元素。则
(1) Al3+的离子结构示意图为![]() ,Cl元素在周期表中位于第ⅦA族;
,Cl元素在周期表中位于第ⅦA族;
(2)C与H组成的化合物有6个原子,即C2H4,其结构简式为CH2=CH2;
(3)铝与氯气形成的化合物为AlCl3,在潮湿的空气中产生白色烟雾是AlCl3发生了水解反应,反应的化学方程式为AlCl3+3H2O=Al(OH)3↓+3HCl↑;
(4) L的最简单气态氢化物甲的水溶液显碱性,所以L为氮元素,甲为NH3,NH3与H2O2反应生成不污染环境的产物,其反应方程式为2NH3+3H2O2=N2↑+6H2O;
(5) 液态CS2在O2中完全燃烧生成两种气态氧化物,反应的化学方程式为CS2+3 O2= CO2+ 2SO2,0.2 mo l CS2完全燃烧生成两种气态氧化物放出热量215 kJ,则反应的热化学方程式为1/5 CS2(l)+3/5 O2(g)=1/5 CO2(g)+2/5 SO2(g);△H=-215 kJ·mol-1,或CS2(l)+3 O2(g)= CO2(g)+2 SO2(g) △H=-1075 kJ·mol-1。


科目:高中化学 来源: 题型:
【题目】铈元素(Ce)是镧系金属中自然丰度最高的一种,常见有+3、+4两种价态,铈的合金耐高温,可以用来制造喷气推进器零件。
请回答下列问题:
(1)雾霾中含有大量的污染物NO,可以被含Ce4+的溶液吸收,生成NO2-、NO3-(二者物质的量之比为1:1),该反应氧化剂与还原剂的物质的量之比为________。
(2)可采用电解法将上述吸收液中的NO2-转化为无毒物质,同时再生Ce4+,其原理如图所示。

①Ce4+从电解槽的______(填字母序号)口流出。
②写出阴极的电极反应式________________。
(3)铈元素在自然界中主要以氟碳矿形式存在。主要化学成分为CeFCO3。工业上利用氟碳铈矿提取CeCl3的一种工艺流程如下:

①焙烧过程中发生的主要反应方程式为__________________。
②有同学认为酸浸过程中用稀硫酸和H2O2替换盐酸更好,他的理由是_________。
③Ce(BF4)3、KBF4的Ksp分别为a、b,则Ce(BF4)3(s)+3KCl(aq)![]() 3KBF4(s)+CeCl3(aq)平衡常数为________(用a、b的代数式表示)。
3KBF4(s)+CeCl3(aq)平衡常数为________(用a、b的代数式表示)。
④加热CeCl3·6H2O和NH4Cl的固体混合物可得固体无水CeCl3,其中NH4Cl的作用是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列氯化物中,既能由金属和氯气直接化合制得,又能由金属和盐酸反应制得的是( )
①CuCl2 ②FeCl2 ③MgCl2 ④ZnCl2
A.③④B.②③C.②③④D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列给定条件的溶液中,一定能大量共存的离子组是( )
A. 无色溶液:Ca2+、H+、Cl-、HSO3-
B. 能使pH试纸呈红色的溶液:Na+、NH4+、Br-、NO3-
C. FeCl2溶液:K+、、Na+、、SO42-、AlO2-
D. 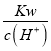 =0.1 mol/L的溶液:Na+、K+、SiO32-、NO3-
=0.1 mol/L的溶液:Na+、K+、SiO32-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个化学反应过程的示意图.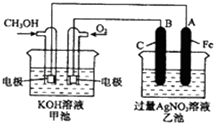
已知甲池的总反应式为:2CH3OH+3O2+4KOH=2K2CO3+6H2O
(1)请回答图中甲、乙两池的名称.甲电池是装置,乙池是装置.
(2)请回答下列电极的名称:通入CH3OH的电极名称是 , B(石墨)电极的名称是 .
(3)写出电极反应式:通入O2的电极的电极反应式是 . A(Fe)电极的电极反应式为 ,
(4)乙池中反应的化学方程式为 .
(5)当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上消耗O2mL(标准状况下)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量。下列反应对应的曲线错误的是
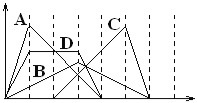
A. 向NaAlO2溶液中滴入HCl至过量
B. 向澄清石灰水中通入CO2至过量
C. 向含有盐酸的A1C13溶液中滴入NaOH溶液至过量。
D. 向含有等物质的量的Ca(OH)2、KOH的混合溶液中通入CO2至沉淀消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中,△H能正确表示物质的燃烧热的是( )
A.CO(g)+ ![]() O2(g)═CO2(g);△H=﹣283.0 kJ/mol
O2(g)═CO2(g);△H=﹣283.0 kJ/mol
B.C(s)+ ![]() O2(g)═CO(g);△H=﹣110.5 kJ/mol
O2(g)═CO(g);△H=﹣110.5 kJ/mol
C.H2(g)+ ![]() O2(g)═H2O(g);△H=﹣241.8 kJ/mol
O2(g)═H2O(g);△H=﹣241.8 kJ/mol
D.2C8H18(l)+25O2(g)═16CO2(g)+18H2O(l);△H=﹣11036 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙三种物质是某抗生素合成过程中的中间产物,下列说法不正确的是
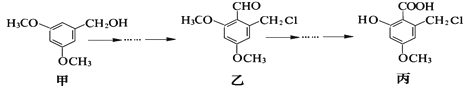
A. 乙、丙都能发生银镜反应
B. 用FeCl3溶液鉴别甲、丙两种有机化合物
C. 甲分子中所有碳原子可能共平面
D. 甲、乙、丙三种有机化合物均可与NaOH溶液发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】计算以下数值(均为25℃时)
(1)某浓度的NH3·H2O溶液中,由水电离的c(H+)=1×10-12mol/L,该溶液的 pH=
(2)将pH=3的H2SO4 溶液和pH=12的NaOH溶液混合, 混合后所得溶液的PH=10,则H2SO4 溶液与NaOH溶液的体积比为
(3)向0.02mol/L的MgCl2溶液中加入NaOH固体,若要生成Mg(OH)2沉淀,溶液的pH最低为(已知Ksp[Mg(OH)2]=3.2×10-11,lg2.5=0.4)
(4)①盐碱地因含较多的 ![]() ,使得土壤呈碱性,不利于作物生长,通过施加适量石膏粉末(主要含有CaSO4 , 微溶于水)来降低土壤的碱性。写出该过程中发生反应的化学方程式
,使得土壤呈碱性,不利于作物生长,通过施加适量石膏粉末(主要含有CaSO4 , 微溶于水)来降低土壤的碱性。写出该过程中发生反应的化学方程式
②SOCl2是一种无色或淡黄色液体,遇水剧烈反应得到二氧化硫和氯化氢,是一种常用的脱水剂。将SOCl2与FeCl36H2O混合并加热,可得到无水FeCl3 , 得到无水FeCl3的化学方程式为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com