
【题目】正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。发生的反应如下:
CH3CH2CH2CH2OH![]() CH3CH2CH2CHO
CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
沸点/。c | 密度/(g·cm-3) | 水中溶解性 | |
正丁醇 | 11.72 | 0.8109 | 微溶 |
正丁醛 | 75.7 | 0.8017 | 微溶 |
实验步骤如下:
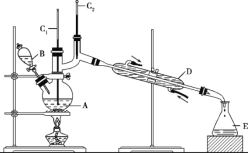
将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中。在A中加入4.0g正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加B中溶液。滴加过程中保持反应温度为90 ~ 95。C,在E中收集90。C以下的馏分。
将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75 ~ 77。C馏分,产量2.0g。
回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,说明理由_______________________。
(2)加入沸石的作用是_____________。若加热后发现未加沸石,应采取的正确方法是__________________。
(3)上述装置图中,B仪器的名称是_________________,D仪器的名称是___________________。
(4)分液漏斗使用前必须进行的操作是_____________(填正确答案标号)。
A.润湿 B.干燥 C.检漏 D.标定
(5)将正丁醛粗产品置于分液漏斗中分水时,水在____________层(填“上”或“下”)
(6)反应温度应保持在90~95。C,其原因是__________________________。
(7)本实验中,正丁醛的产率为___________%。
【答案】
(1)不能,易迸溅;
(2)防止暴沸;冷却后补加;
(3)滴液漏斗;直形冷凝管;
(4)C;(5)下;
(6)既可保证正丁醛及时蒸出,又可尽量避免其被进一步氧化;
(7)51.3℅;
【解析】
试题分析:(1)不能将Na2Cr2O7溶液加到浓硫酸中,应该将浓硫酸加到Na2Cr2O7溶液,因为浓硫酸溶于水会放出大量热,容易溅出伤人,故答案为:不能,浓硫酸溶于水会放出大量热,容易溅出伤人;
(2)沸石的作用是防止液体暴沸,若加热后发现未加沸石,应采取的正确方法是冷却后补加,以避免加热时继续反应而降低产率,故答案为:防止液体暴沸;冷却后补加;
(3)B仪器是分液漏斗,D仪器是冷凝管,故答案为:分液漏斗;冷凝管;
(4)分液漏斗使用前必须检查是否漏水,应选c,故答案为:c;
(5)因为正丁醛的密度是0.801 7gcm-3,比水轻,水层在下层,故答案为:下;
(6)反应温度应保持在90~95℃,根据正丁醛的沸点和还原性,主要是为了将正丁醛及时分离出来,促使反应正向进行,并减少正丁醛进一步氧化,故答案为:为了将正丁醛及时分离出来,促使反应正向进行,并减少正丁醛进一步氧化;
(7)按反应关系,正丁醛的理论产量是:4.0g![]() =3.9g,实际产量是2.0g,产率为:
=3.9g,实际产量是2.0g,产率为:![]() ×100%=51.3%,故答案为:51.3。
×100%=51.3%,故答案为:51.3。


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:
【题目】
A. 同一生物体不同组织细胞内化学元素种类和含量大体相同
B. C、H、O、N是组成生物体内酶所必需的元素
C. 蛋白质中的S元素存在于氨基酸的R基中
D. 占细胞的鲜重最多的元素是O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验是化学研究的基础.下列关于各实验装置的叙述正确的是( )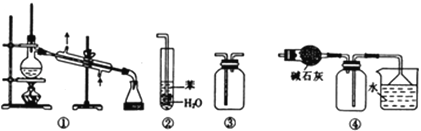
A. 装置①常用于分离互不相溶的液体混合物
B. 装置②可用于吸收NH3或HCl气体,并防止倒吸
C. 装置③可用于收集H2、CO2、Cl2、NH3等气体
D. 装置④可用于干燥、收集氯化氢,并吸收多余的氯化氢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)某气态氧化物化学式为RO2,在标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为____________,R的相对原子质量为____________。
(2)已知CO、CO2的混合气体的质量为15 g,在标准状况下体积为8.8 L,则可推知该混合气体中含CO________ g,所含CO2在标准状况下体积为____________ L。
(3)将4 g NaOH溶于____________g水中,才能使每100个水分子中溶有1个Na+。
(4)同温同压下SO2 与 He密度之比为 ,若质量相等,两种气体的体积之比____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在生产和生活中有着重要的应用。下列说法正确的是 ( )
A.“雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮的氧化物无关
B.“辽宁舰”上用于舰载机降落拦阻索的特种钢缆属于新型无机非金属材料
C.白酒中混有少量塑化剂,可通过过滤除去
D.能够改善食品的色、香、味,并有防腐、保鲜作用的食品添加剂应限量使用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案设计中,可行的是( )
A. 加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铝粉
B. 用萃取的方法分离汽油和煤油
C. 用溶解、过滤的方法分离KNO3和NaCl固体的混合物
D. 将O2和H2的混合气体通过灼热的氧化铜,以除去其中的H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓H2SO4 密度1.84g/mL,物质的量浓度为18.4mol/L,质量分数为98%,取10mL浓H2SO4和a mL水混合得物质的量浓度为C mol/L,质量分数为b%.下列组合正确的是( )
(1)若C=9.2则a>10 b>49%
(2)若C=9.2则a>10 b<49%
(3)若b=49则a=18.4 C<9.2
(4)若b=49则a=18.4 C>9.2.
A.(1)(3) B.(1)(4) C.(2)(3) D.(2)(4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羟胺(![]() )是一种还原剂.现用
)是一种还原剂.现用![]() 的羟胺的酸性溶液跟足量的
的羟胺的酸性溶液跟足量的![]() 溶液在煮沸条件下反应,生成
溶液在煮沸条件下反应,生成![]() 离子恰好与
离子恰好与![]()
![]() 的酸性
的酸性![]() 溶液完全作用生成
溶液完全作用生成![]() ,
,![]() 等物质,则上述反应中羟胺的氧化产物是
等物质,则上述反应中羟胺的氧化产物是
A.![]() B.
B.![]() C.NO D.
C.NO D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A. 1 mol 氧气中含有12.04×1023个氧原子,在标准状况下占有体积22.4 L
B. 1 mol臭氧和1.5 mol氧气含有相同的氧原子数
C. 等体积、浓度均为1 mol/L的磷酸和盐酸,电离出的氢离子数之比为3∶1
D. 等物质的量的干冰和葡萄糖(C6H12O6)中所含碳原子数之比为1∶6,氧原子数之比为1∶3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com