
在密闭容器中充入N2和H2,合成NH3,到2秒末测得,v (H2) =0.45 mol / (L·s),则2秒末NH3的浓度为( )
A. 0.9 mol / L B. 0.45 mol / L C. 0.6 mol / L D. 0.55 mol / L
科目:高中化学 来源: 题型:
苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:

制备苯乙酸的装置示意图如下(加热和夹持装置等略):

已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
。
(2)将a中的溶液加热至100 ℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130 ℃继续反应。在装置中,仪器b的作用是 ;仪器c的名称是 ,其作用是 。
反应结束后加适量冷水,再分离出苯乙酸粗品。加人冷水的目的是 。下列仪器中可用于分离苯乙酸粗品的是 (填标号)。
A.分液漏斗 B.漏斗 C.烧杯 D.直形冷凝管 E.玻璃棒
(3)提纯粗苯乙酸的方法是 ,最终得到44 g纯品,则苯乙酸的产率是 。
(4)用CuCl2 • 2H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是 。
(5)将苯乙酸加人到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:将Cl2通入适量KOH溶液,产物中可能有KC1、KClO、KC1O3,且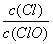 的值与温度高低有关。当n(KOH)=amol时,下列有关说法错误的是
的值与温度高低有关。当n(KOH)=amol时,下列有关说法错误的是
A、若某温度下,反应后c(Cl-):c(ClO-)=11,则溶液中c(ClO-):c(ClO3-)=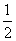
B、参加反应的氯气的物质的量等于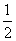 amol
amol
C、改变温度,反应中转移电子的物质的量n的范围: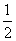 amol≤n≤
amol≤n≤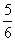 amol
amol
D、改变温度,产物中KC1O3的最大理论产量为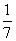 amol
amol
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏伽德罗常数的数值,下列叙述正确的是
A.常温下,1mol丙烯中含碳原子数为3NA
B.常温下,pH=13的 NaOH溶液中含OH-数为NA
C.标准状况下,22.4LCHCl3中含C-H键数为NA
D.23g Na与足量氧气反应时转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F为前四周期元素且原子序数依次增大,其中A含有3个能级,且每个能级所含的电子数相同;C的最外层有6个运动状态不同的电子;D是短周期元素中电负性最小的元素;E的最高价氧化物对应的水化物酸性最强;F除最外层原子轨道处于半充满状态,其余能层均充满电子。G元素与D元素同主族,且相差3个周期。
(1)元素A、B、C的电负性由小到大的顺序是________(用元素符号表示)。
(2)E的最高价含氧酸中E的杂化方式为________。
(3)F原子的外围电子排布式为________,F的晶体中原子的堆积方式是下图中的________(填“甲”“乙”或“丙”)。

(4)D与E、G与E形成的晶体类型相同,但晶体的配位数不同,其原因是____________________________________________________________ __________。
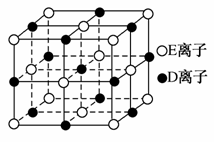
(5)已知DE晶体的晶胞如图所示。若将DE晶胞中的所有E离子去掉,并将D离子全部换为A原子,再在其中的4个“小立方体”中心各放置一个A原子,且这4个“小立方体”不相邻。位于“小立方体”中的A原子与最近的4个原子以单键相连,由此表示A的一种晶体的晶胞(已知A—A键的键长为a cm,NA表示阿伏加德罗常数),则该晶胞中含有________个A原子,该晶体的密度是________g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
在常温下,将等体积的盐酸和氨水混和后,所得溶液的pH=7,则下列说法正确的是 ( )
A. 原来盐酸的物质的量浓度等于氨水的物质的量浓度
B. 所得溶液中c(NH4+)=c(Cl—)
C. 所得溶液中c(NH4+)+c(H+)=c(Cl—)
D. 所得溶液中c(NH4+)+c(NH3·H2O)=c(Cl—)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学反应速率的说法不正确的是 ( )
A.化学反应达到最大限度时,正逆反应速率也达到最大且相等
B.催化剂能降低化学反应的活化能,加快反应速率,提高生产效率
C.用锌和稀硫酸反应制取H2时,滴加几滴硫酸铜溶液能加快反应速率
D.用铁片和稀硫酸反应制H2比用98%的浓硫酸产生H2的速率快
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)用18 mol/L的硫酸配制100 mL 1.0 mol/L的硫酸,若实验仪器有:A.100 mL量筒 B.托盘天平 C.玻璃棒 D.50 mL容量瓶 E.25 mL酸式滴定管 F.胶头滴管 G.50 mL烧杯 H.100 mL容量瓶
实验时所需仪器的先后顺序是(填入编号)____________________________________。
(2)在容量瓶的使用方法中,下列操作不正确的是(填写编号)________。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线1 cm~2 cm处,用滴管滴加蒸馏水到标线
D.配制溶液时,如果试样是液体,用滴定管量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近标线1 cm~2 cm处,用滴管滴加蒸馏水到标线
E.盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转或摇动多次
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com