
| A、使用防腐剂延长食品保质期 |
| B、利用风力发电,获取清洁能源 |
| C、研发可降解塑料,控制白色污染 |
| D、将汽车尾气中的NO和CO转化为无害气体 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2(V-W)升 |
| B、(2V-W)升 |
| C、(V-W)升 |
| D、2W 升 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 操作 | 现象 | 解释或推论 |
| A | 铁片投入浓硫酸 | 无明显变化 | 常温下铁不与浓硫酸反应 |
| B | 将浓硫酸滴到白纸上 | 白纸变黑 | 浓硫酸强氧化性导致纸张中的纤维素炭化 |
| C | 二氧化硫通入溴水 | 溴水褪色 | 说明二氧化硫具有漂白性 |
| D | 试纸检验某气体 | 试纸变蓝 | 该气体是氨气 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:2 | B、8:1 |
| C、16:207 | D、71:216 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、铝粉投入到NaOH溶液中:2Al+2OH-=2AlO
| ||
| B、BaCO3和盐酸:BaCO3+2H+=Ba2++CO2↑+H2O | ||
| C、铜与盐酸反应:Cu+2H+=Cu2++H2↑ | ||
| D、AlCl3溶液中加入足量的氨水:Al3++3OH-=Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
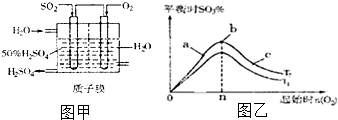 国家拟于“十二五”期间将SO2的排放量减少8%,研究SO2综合利用意义重大.
国家拟于“十二五”期间将SO2的排放量减少8%,研究SO2综合利用意义重大.| 1 |
| x |
| 3 |
| x |
查看答案和解析>>
科目:高中化学 来源: 题型:


| NH3?H2O | Kb=1.8×10-5mol?L-1 |
| H2SO3 | Ka1=1.2×10-2mol?L-1 Ka2=1.3×10-8mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 溶液 | 操作及现象 |
| A | CaC12溶液 | 通入CO2,溶液不变浑浊;再通入氨气,溶液变浑浊 |
| B | Na2SiO3溶液 | 通入CO2,溶液变浑浊;继续通CO2至过量,浑浊消失 |
| C | Ca(C1O)2溶液 | 通入CO2,溶液变浑浊;再加入品红溶液,红色不褪去 |
| D | BaC12溶液 | 先通入NO2,再通入SO2至过量,先生成沉淀后沉淀消失 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com