
| A. | MgF2晶体中的化学键是共价键 | |
| B. | 在共价化合物中一定存在共价键 | |
| C. | N2和CH4两种分子中,每个原子的最外层都具有8电子稳定结构 | |
| D. | 离子化合物一定只含离子键 |
分析 A.MgF2晶体只含离子键;
B.共价化合物中一定不含离子键,含离子键的一定为离子化合物;
C.CH4中H原子的最外层为2电子;
D.离子化合物中含离子键,可能含共价键.
解答 解:A.MgF2晶体只含离子键,不含共价键,故A错误;
B.共价化合物中一定不含离子键,含离子键的一定为离子化合物,则在共价化合物中一定存在共价键,故B正确;
C.CH4中H原子的最外层为2电子,而C及氮气中N的最外层都具有8电子稳定结构,故C错误;
D.离子化合物中含离子键,可能含共价键,如NaOH中含共价键,故D错误;
故选B.
点评 本题考查共价键,为高频考点,把握共价键的形成及判断为解答的关键,侧重分析与应用能力的考查,注意常见物质中的化学键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 原子半径大小顺序为M>W>X>Z>Y | |
| B. | W元素形成的可溶性盐溶液一定显碱性 | |
| C. | M、X只能形成离子化合物,且形成的离子化合物中只含离子键 | |
| D. | W的氧化物与Z、M的最高价氧化物的水化物均能反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
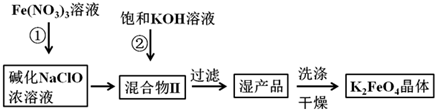
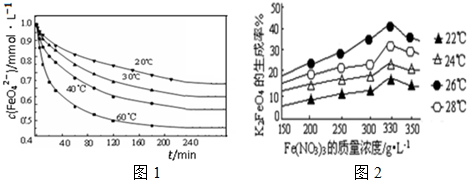
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑥⑦ | B. | ①⑦ | C. | ①②⑥ | D. | ①⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
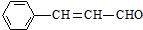 ,则关于该有机物的说法正确的是( )
,则关于该有机物的说法正确的是( )| A. | 1 mol该有机物发生银镜反应能生成 1 mol Ag | |
| B. | 1 mol该有机物最多能够与4 mol H2 发生加成反应 | |
| C. | 它与 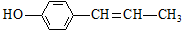 互为同分异构体 互为同分异构体 | |
| D. | 该有机物能使高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用灼烧的方法可以区分蚕丝和人造纤维 | |
| B. | 用浸泡有高锰酸钾溶液的硅藻土吸收水果释放出的乙烯,可以达到水果保鲜的目的 | |
| C. | 加热能杀死流感病毒是因为蛋白质受热变性 | |
| D. | 医用消毒酒精中乙醇的浓度为95% |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 一段时间负极质量明显减轻 | |
| B. | 电子通过导线由铜片流向锌片 | |
| C. | 只有正极上有氢气逸出,正极电极反应式为:2H++2e-═H2↑ | |
| D. | 正极附近的SO42-离子浓度逐渐增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属性:K>Na>Li | B. | 酸性:HClO3>H2SO4>H3PO4 | ||
| C. | 还原性:I->Br->Cl- | D. | 氧化性:F2>Cl2>Br2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com