
【题目】DDT又叫滴滴涕,化学名为双对氯苯基三氯乙烷,化学式(ClC6H4)2CH(CCl3)。名称从英文缩写DDT而来,为白色晶体,不溶于水,溶于煤油,可制成乳剂,是有效的杀虫剂。DDT进入食物链,是导致一些食肉和食鱼的鸟接近灭绝的主要原因。因此从70年代后滴滴涕逐渐被世界各国明令禁止生产和使用。其结构为: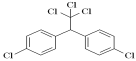 ,下列有关说法正确的是 ( )
,下列有关说法正确的是 ( )
A. 属于烃类 B. DDT完全燃烧后只产生CO2和H2O两种物质
C. 分子无手性碳 D. 氢核磁共振谱图中有5种位置峰
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】我国是干电池的生产和消费大国。某科研团队设计了以下流程对废旧碱性锌锰干电池的资源进行回收:

已知:
①Ksp(MnS)=2.5×10-13,Ksp(ZnS)=1.6×10-24
②Mn(OH)2开始沉淀时pH为8.3,完全沉淀的pH为9.8
③ 0.1 mol/L NaHCO3溶液的pH约为8;0.1 mol/L Na2CO3溶液的pH约为11。
(1)碱性锌锰干电池是以锌粉为负极,二氧化锰为正极,氢氧化钾溶液为电解质。电池总反应为:2MnO2+Zn+2KOH= 2MnOOH+K2ZnO2,请写出电池的正极反应式________________________________;
(2)为了提高碳包的浸出效率,可以采取的措施有______________________________;(写一条即可)
(3)向滤液1中加入MnS的目的是__________________________________________;
(4)已知MnSO4的溶解度曲线如图所示,从滤液2中析出MnSO4·H2O晶体的操作是蒸发结晶、____________________、洗涤、低温干燥;

(5)为了选择试剂X,在相同条件下,分别用3 g碳包进行制备MnSO4的实验,得到数据如下表,请写出最佳试剂X与碳包中的主要成分发生反应的化学方程式________________。
实验编号 | 试剂X | MnSO4/g |
1 | 锌粉 | 2.4 |
2 | 铁粉 | 2.7 |
3 | FeS粉末 | 3.0 |
4 | 30%过氧化氢 | 3.7 |
(6)工业上经常采用向滤液2中加入NaHCO3溶液来制备MnCO3,不选择Na2CO3溶液的原因是_______________________________________;
(7)该科研小组利用EDTA(乙二胺四乙酸二钠,阴离子简写为Y2-)进行络合滴定,测定Mn元素在电池中的质量百分数。
实验过程如下:
①将一节废旧碱性锌锰干电池拆解后,去除金属、碳棒以及外包装后;
②准确称取固体粉末1.200 g;
③经过水浸…等步骤得到滤液1(<100 mL);
④将滤液1稀释至100.00 mL;
⑤取20.00 mL溶液用0.0500 molL-1EDTA标准溶液滴定;在一定条件下,只发生反应:Mn2++Y2-=MnY。
⑥重复滴定3次,平均消耗标准溶液22.00 mL。
则Mn元素的质量百分数为________。(保留3位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A. pH=7的溶液:K+、Na+、Cl-、Fe3+
B. 能使酚酞显红色的溶液:Na+、Mg2+、HCO3-、SO42-
C. c(H+)/c(OH-)=1012的溶液:K+、Fe3+、Cl-、SO42-
D. 水电离出的c(H+)=10-13 mol·L-1的溶液:Ca2+、NH4+、NO3-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:CO(g)+2H2(g) ![]() CH3OH(g) ΔH
CH3OH(g) ΔH

(1)根据图1请写出合成甲醇的热化学方程式_______________(热量用E1、E2或E3表示)。
(2)该反应的逆反应速率随时间变化的关系如上图2。t1时改变了某种条件,改变的条件可能是________________________。
(3)判断反应达到平衡状态的依据是____________(填字母序号)。
A.2v(H2)(逆) =v(CO)(正)
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
E.容器内CO、H2、CH3OH的浓度之比为1:2:1
(4)在一定温度下,若将4a mol H2和2amol CO放入2L的密闭容器中,充分反应后测得CO的转化率为50%,则该反应的平衡常数为___________。若此时再向该容器中投入a mol CO、2amol H2和amol CH3OH,判断平衡移动的方向是_____________(“正向移动”“逆向移动”或“不移动”);与原平衡相比,CO的物质的量浓度__________(填“增大”、“不变”或“减小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l)△H1
2 H2(g)+ O2(g)= 2H2O(g)△H2
C(s)+ O2(g)=CO2(g)△H3
则反应4C3H5(ONO2)3(l)= 12CO2(g)+10H2O(g) + O2(g) +6N2(g)的△H为
A. 12△H3+5△H2-2△H1 B. 2△H1-5△H2-12△H3
C. 12△H3-5△H2-2△H1 D. △H1-5△H2-12△H3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com