
| ��� | ��Ӧ | ƽ�ⳣ�� |
| 1 | Au+6HNO3��Ũ��=Au��NO3��3+3NO2��+3H2O | ����1 |
| 2 | Au3++4Cl-=AuCl4- | ����1 |

 =
=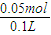 =0.5 mol/L���������Ӻ��������Ʒ�Ӧ�����������������ڿ����и��ױ�����Ϊ�������������ȷֽ����ɵ���������������4.8g������ԭ���غ㣬�������ӵ����ʵ����ǣ�
=0.5 mol/L���������Ӻ��������Ʒ�Ӧ�����������������ڿ����и��ױ�����Ϊ�������������ȷֽ����ɵ���������������4.8g������ԭ���غ㣬�������ӵ����ʵ����ǣ� ×2
×2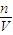 =
= =0.6mol/L���ʴ�Ϊ��0.5��0.6��
=0.6mol/L���ʴ�Ϊ��0.5��0.6��

 ��������ϵ�д�
��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��� | ��Ӧ | ƽ�ⳣ�� |
| 1 | Au+6HNO3��Ũ��=Au��NO3��3+3NO2��+3H2O | ����1 |
| 2 | Au3++4Cl-=AuCl4- | ����1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| ��� | ��Ӧ | ƽ�ⳣ�� |
| �� | Au+6HNO3��Ũ��?Au��NO3��3+3NO2+3H2O | ����1 |
| �� | Au3++4Cl-?AuCl4- | ����1 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ��� | ��Ӧ | ƽ�ⳣ�� |
| 1 | Au+6HNO3��Ũ���TAu��NO3��3+3NO2��+3H2O | ����1 |
| 2 | Au3++4Cl-�TAuCl4- | ����1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��ɽ��ʡ��ׯ��2010������꼶���п������ۣ���ѧ���֣����� ���ͣ������
��8�֣�[��ѧ����ѧ�뼼��]
��ͭ�к���������п������������Ƚ����������������ʣ������Ӧ������ʵ����������������ͭ��ҺΪ���Һ���õ��ķ����Դ�ͭ�ᴿ������������͵��Һ�н������л��պͺ����ⶨ���ش��������⣻
��1������һ����⾫�ƣ��������У�����ͭ��Ũ�Ȼ� ��ѡ�����䡢��С����
������������ɺԵ��Һ���д�����
��2����������ۺ����ã�
ϡ���ᴦ��������õ�������ϡ��Һ����д���ò���Ӧ�����ӷ���ʽ�� ��
�������м������Ļƽ���λ��ս����Dz������й����ϣ��˽��һЩ�йؽ��֪ʶ�����������ǻ�ȡ��һЩ��Ϣ��
|
��� |
��Ӧ |
ƽ�ⳣ�� |
|
1 |
Au + 6HNO3��Ũ��= Au(NO3)3 + 3NO2��+ 3H2O |
<< 1 |
|
2 |
Au3+ + 4Cl�� = AuCl4�� |
>>1 |
���п�֪������������ᷴӦ����ȴ��������ˮ��Ũ���������ᰴ�����l��3�Ļ����������Ҫ���ͽ��ܹ�������ˮ��ԭ�� ��
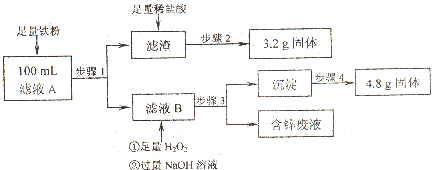
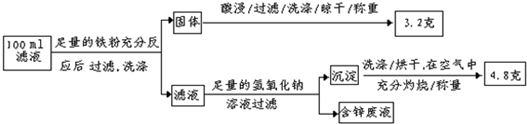
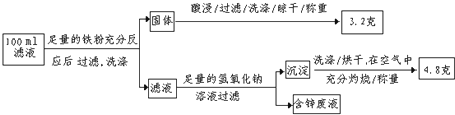
��3�����Һ�����IJⶨ����ͼ�Ǹ�С��̽�����Һ��һ��ʵ�����̣�
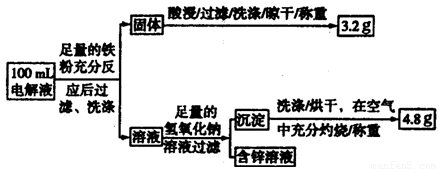
��100mL��Һ��Cu2+ ��Ũ��Ϊ mol��L��1 ��Fe2+��Ũ��Ϊ mol��L��1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com