
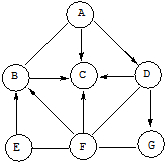
 ŌņŌ»ģŗĻĪļÖŠE”¢GµÄĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ1£®
ŌņŌ»ģŗĻĪļÖŠE”¢GµÄĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ1£® ·ÖĪö A”«GŹĒ³õÖŠ»Æѧ³£¼ūµÄ“æ¾»Īļ£¬EŹĒ·¢½Ķ·ŪµÄÖ÷ŅŖ³É·Ö£¬ŌņEĪŖNaHCO3£¬B”¢CŹĒŃõ»ÆĪļ£¬A”«GŹĒ¾łŗ¬ÓŠŅ»ÖÖĻąĶ¬µÄŌŖĖŲ£¬Ōņ¾łŗ¬ÓŠOŌŖĖŲ£¬ŌņBĪŖCO2£¬CĪŖH2O£¬AµÄ±„ŗĶČÜŅŗ¼ÓČČŗó»į±ä»ė×Ē£¬ŌņAĪŖCa£ØOH£©2£¬F·“Ó¦æÉŅŌµĆµ½¶žŃõ»ÆĢ¼ÓėĖ®£¬ŌņFĪŖĖį£¬¹ŹFĪŖH2SO4£¬E”¢G·Ö±šÓė×ćĮæF·“Ó¦µÄÉś³ÉĪļĻąĶ¬£¬ŌņGĪŖNa2CO3£¬D·“Ó¦æÉŅŌµĆµ½Ė®”¢Ģ¼ĖįĒāÄĘ£¬A·“Ó¦æÉŅŌµĆµ½G£¬ŌņGĪŖNaOH£¬¾Ż“Ė½ā“š£®
½ā“š ½ā£ŗA”«GŹĒ³õÖŠ»Æѧ³£¼ūµÄ“æ¾»Īļ£¬EŹĒ·¢½Ķ·ŪµÄÖ÷ŅŖ³É·Ö£¬ŌņEĪŖNaHCO3£¬B”¢CŹĒŃõ»ÆĪļ£¬A”«GŹĒ¾łŗ¬ÓŠŅ»ÖÖĻąĶ¬µÄŌŖĖŲ£¬Ōņ¾łŗ¬ÓŠOŌŖĖŲ£¬ŌņBĪŖCO2£¬CĪŖH2O£¬AµÄ±„ŗĶČÜŅŗ¼ÓČČŗó»į±ä»ė×Ē£¬ŌņAĪŖCa£ØOH£©2£¬F·“Ó¦æÉŅŌµĆµ½¶žŃõ»ÆĢ¼ÓėĖ®£¬ŌņFĪŖĖį£¬¹ŹFĪŖH2SO4£¬E”¢G·Ö±šÓė×ćĮæF·“Ó¦µÄÉś³ÉĪļĻąĶ¬£¬ŌņGĪŖNa2CO3£¬D·“Ó¦æÉŅŌµĆµ½Ė®”¢Ģ¼ĖįĒāÄĘ£¬A·“Ó¦æÉŅŌµĆµ½G£¬ŌņGĪŖNaOH£®
£Ø1£©CµÄ»ÆѧŹ½ĪŖH2O£¬¹Ź“š°øĪŖ£ŗH2O£»
£Ø2£©BŗĶCµÄ»ģŗĻĪļĪŖĢ¼ĖįČÜŅŗ£¬µĪ¼ÓĪŽÉ«·ÓĢŖČÜŅŗ£¬·ÓĢŖČÜŅŗĻŌĪŽÉ«£¬¹Ź“š°øĪŖ£ŗĪŽÉ«£»
£Ø3£©FŗĶD·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2NaOH+H2SO4=Na2SO4+2H2O£¬¹Ź“š°øĪŖ£ŗ2NaOH+H2SO4=Na2SO4+2H2O£»
£Ø4£©NaHCO3”¢Na2CO3µÄ»ģŗĻĪļ19g£¬½«ĘäÓė×ćĮæĮņĖįČÜŅŗ·“Ó¦²śÉś±ź×“æöĻĀµÄĘųĢå4.48L£¬¼“Éś³É¶žŃõ»ÆĢ¼ĪŖ$\frac{4.48L}{22.4L/mol}$=0.2mol£¬ÉčNaHCO3”¢Na2CO3µÄĪļÖŹµÄĮæ·Ö±šĪŖxmol”¢ymol£¬Ōņ£ŗ
$\left\{\begin{array}{l}{x+y=0.2}\\{84x+106y=19}\end{array}\right.$
½āµĆx=y=0.1
ŌņŌ»ģŗĻĪļÖŠNaHCO3”¢Na2CO3µÄĪļÖŹµÄĮæÖ®±ČĪŖ0.1mol£ŗ0.1mol=1£ŗ1£¬
¹Ź“š°øĪŖ£ŗ1£ŗ1£®
µćĘĄ ±¾Ģāæ¼²éĪŽ»śĪļĶʶĻ£¬»ł±¾ŹōÓŚ²Ā²āŃéÖ¤ŠĶĢāÄ棬עŅāĢāÄæĻŽÖĘĪŖ³õÖŠ³£¼ūĪļÖŹ£¬”°AµÄ±„ŗĶČÜŅŗ¼ÓČČŗó»į±ä»ė×Ē£¬B”¢CŹĒŃõ»ÆĪļ£¬EŹĒ·¢½Ķ·ŪµÄÖ÷ŅŖ³É·Ö”±ŹĒĶʶĻĶ»ĘĘæŚ£¬ÄѶČÖŠµČ£®


 ÓÅŠćÉśÓ¦ÓĆĢāæØæŚĖćĢģĢģĮ·ĻµĮŠ“š°ø
ÓÅŠćÉśÓ¦ÓĆĢāæØæŚĖćĢģĢģĮ·ĻµĮŠ“š°ø Õć½Ö®ŠĒæĪŹ±ÓÅ»Æ×÷ŅµĻµĮŠ“š°ø
Õć½Ö®ŠĒæĪŹ±ÓÅ»Æ×÷ŅµĻµĮŠ“š°ø ¼¤»īĖ¼Ī¬ÓżÓæĪĢĆĻµĮŠ“š°ø
¼¤»īĖ¼Ī¬ÓżÓæĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 4.48L | B£® | 5.6L | C£® | 6.72L | D£® | 8.96L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | $\frac{c£Ø{H}^{+}£©}{c£ØO{H}^{-}£©}$=1”Į1014µÄČÜŅŗ£ŗCa2+”¢Na+”¢ClO-”¢NO3- | |
| B£® | 1.0mol•L-1µÄKNO3ČÜŅŗ£ŗH+”¢Fe2+”¢Cl-”¢SO42- | |
| C£® | ŗ¬ÓŠ0.1mo•L-1µÄCa2+ČÜŅŗ£ŗNa+”¢K+”¢CO32-”¢Cl- | |
| D£® | ³ĪĒåĶøĆ÷µÄČÜŅŗÖŠ£ŗNa+”¢K+”¢MnO4-”¢AlO2- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÅäÖĘ5%µÄŹ³ŃĪČÜŅŗŹ±£¬½«³ĘĮæµÄŹ³ŃĪ·ÅŌŚÉÕ±ÖŠ¼ÓŹŹĮæµÄÕōĮóĖ®½Į°čČܽā | |
| B£® | ÓĆĖįŹ½µĪ¶Ø¹Ü×¼Č·ĮæČ”10.00 mL KMnO4ČÜŅŗ | |
| C£® | ÓĆ500 mLČŻĮæĘæÅäÖĘ1 mol/LµÄNaOHČÜŅŗ | |
| D£® | ÓĆpHŹŌÖ½²āµĆŠĀÖĘĀČĖ®µÄpHĪŖ2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¹čµ„ÖŹ¼Č²»ÄÜÓėĖį·“Ó¦ÓÖ²»ÄÜÓė¼ī·“Ó¦ | |
| B£® | ¾§Ģå¹čÖŠĆæøö¹čŌ×ÓÓėĮķĶāĖÄøö¹čŌ×ÓŠĪ³É4øö¹²¼Ū¼ü | |
| C£® | ¹čÓėNaOHČÜŅŗµÄ·“Ó¦ÖŠNaOH×÷Ńõ»Æ¼Į | |
| D£® | ¹čŌŖĖŲŌŚµŲæĒÖŠµÄŗ¬Įæ¾ÓµŚŅ»Ī» |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
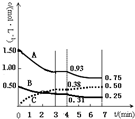 ÓŠA”¢B”¢CČżÖÖĘųĢåŌŚŅ»øö¹Ģ¶ØČŻ»żµÄČŻĘ÷ÖŠ·¢Éś·“Ó¦£¬ĢåĻµÖŠø÷ĪļÖŹÅضČĖꏱ¼ä±ä»ÆµÄĒśĻßČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
ÓŠA”¢B”¢CČżÖÖĘųĢåŌŚŅ»øö¹Ģ¶ØČŻ»żµÄČŻĘ÷ÖŠ·¢Éś·“Ó¦£¬ĢåĻµÖŠø÷ĪļÖŹÅضČĖꏱ¼ä±ä»ÆµÄĒśĻßČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ3A£Øg£©+B£Øg£©ØT2C£Øg£© | |
| B£® | Čō½«³õŹ¼Ķ¶·ÅµÄĪļÖŹÅضČŌöÖĮŌĄ“µÄ2±¶£¬Ōņ·“Ó¦ĪļµÄ×Ŗ»ÆĀŹŌö“ó£¬Ę½ŗā³£Źż²»±ä | |
| C£® | ČōµŚ4 min Ź±½µµĶĪĀ¶Č£¬µ½7 minŹ±“ļµ½ĮĖŠĀµÄĘ½ŗā£¬Ōņ“Ė·“Ó¦µÄ”÷H£¼0 | |
| D£® | ·“Ó¦ŌŚĒ°3 minµÄĘ½¾ł·“Ó¦ĖŁĀŹ¦Ō£ØA£©=0.31mol•L-1•min-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
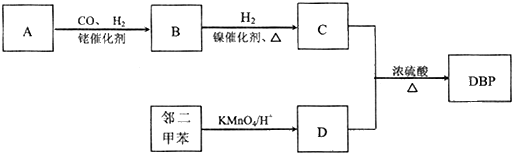
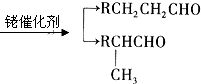
 £®
£®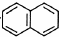 £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com