
【题目】化学与人类生产和生活中密切相关,掌握有关的化学基础知识可以改善我们的生活.
日常生活中使用的各种电池就是利用化学反应将化学能转化为电能,各种各样的电池的发展是化学对人类的一项重大贡献.请回答下列有关化学电源的问题:
(1)下列有关电池的叙述中正确的是 .
A.锌锰干电池工作一段时间后碳棒变细
B.氢氧燃料电池可将热能直接转变为电能
C.甲烷燃料电池工作时甲烷在负极被氧化
D.太阳能电池的主要材料是高纯度的二氧化硅
(2)锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过.下列叙述正确的是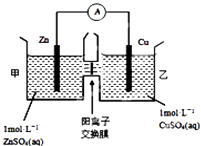
A.铜电极上发生氧化反应
B.电池工作一段时间后,甲池的c(SO42﹣)减小
C.电池工作一段时间后,乙池溶液的总质量增加
D.甲池中的阳离子向乙池移动,保持溶液中电荷平衡
(3)航天技术上使用的氢一氧燃料电池具有高能、轻便和不污染环境等优点.氢一氧燃料电池有酸式和碱式两种,它们放电时的电池总反应式都可表示为2H2+O2=2H2O.酸式氢一氧燃料电池的电解质是酸,放电时其正极的电极反应可表示为 , 放电一段时间后电解质溶液的酸性将(填“增强”、“减弱”、“不变”).
(4)根据已学知识回答下列问题:
已知拆开1mol H﹣H键,1mol N﹣H键,1mol N≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为 .
(5)用高铁酸钾和锌制成的高铁碱性电池,能储存比普通碱性电池多50%的电能,己知该电池的总反应为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2 , 则负极的电极反应为 .
【答案】
(1)C
(2)C,D
(3)O2+4e﹣+4H+=2H2O;减弱
(4)N2(g)+3H2(g)?2NH3(g)△H=﹣92kJ?mol﹣1
(5)Zn﹣2e﹣+2OH﹣=ZnO+H2O
【解析】解:(1)A.锌锰干电池碳棒不发生变化,起到导电作用,故A错误;B.氢氧燃料电池可将化学能直接转变为电能,故B错误;C.甲烷燃料电池工作时甲烷在负极被氧化,氧气为正极,故C正确;D.太阳能电池的主要材料是高纯度的硅,故D错误.所以答案是:C;
(2.)A.由图象可知,该原电池反应式为:Zn+Cu2+=Zn2++Cu,Zn为负极,发生氧化反应,Cu为正极,发生还原反应,故A错误;B.阳离子交换膜只允许阳离子和水分子通过,故两池中c(SO42﹣)不变,故B错误;C.甲池中的Zn2+通过阳离子交换膜进入乙池,乙池中发生反应:Cu2++2e﹣=Cu,保持溶液呈电中性,进入乙池的Zn2+与放电的Cu2+的物质的量相等,而Zn的摩尔质量大于Cu,故乙池溶液总质量增大,故C正确;D.甲池中的Zn2+通过阳离子交换膜进入乙池,以保持溶液电荷守恒,乙池消耗铜,溶液质量增大,故D正确,所以答案是:CD;
(3.)氢氧燃料电池无论是酸性还是碱式性,其电池总反应均为:2H2+O2=2H2O ①,酸性氢氧燃料电池负极电极反应式为:2H2﹣4e﹣=4H+②,用(①﹣②)即得酸性氢氧燃料电池的正极反应:O2+4H++4e﹣=2H2O,溶液体积增大,氢离子浓度减小,酸性减弱,所以答案是:O2+4e﹣+4H+=2H2O;减弱;
(4.)在反应N2+3H22NH3中,断裂3molH﹣H键,1mol N三N键共吸收的能量为:3×436kJ+946kJ=2254kJ,生成2mol NH3 , 共形成6mol N﹣H键,放出的能量为:6×391kJ=2346kJ,吸收的能量少,放出的能量多,该反应为放热反应,放出的热量为:2346kJ﹣2254kJ=92kJ,即N2(g)+3H2(g)2NH3(g)△H=﹣92kJmol﹣1 , 所以答案是:N2(g)+3H2(g)2NH3(g)△H=﹣92kJmol﹣1;
(5.)由总方程式可知负极锌被氧化生成氧化锌,电极方程式为Zn﹣2e﹣+2OH﹣=ZnO+H2O,所以答案是:Zn﹣2e﹣+2OH﹣=ZnO+H2O.


 小学教材全测系列答案
小学教材全测系列答案科目:高中化学 来源: 题型:
【题目】某混合溶液中,可能大量含有的离子如下表:
阳离子 | H+、K+、Al3+、NH4+、Mg2+ |
阴离子 | OH-、SO42-、CO32-、AlO2- |
将Na2O2逐渐加入上述混合溶液中并微热(忽略溶液体积变化及水蒸气的影响),产生沉淀和气体如图所示。
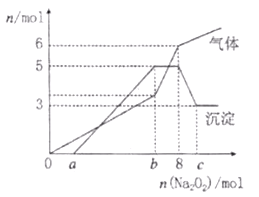
请根据信息回答下列问题:
(1)将上述混合溶液中一定大量含有的阴、阳离子及其物质的量填入下表(可以不填满,也可以增加):____
离子种类 | ||||||
物质的量(mol) |
(2)图中a=____;b=____;c=____.
(3)简述溶液中还可能大量含有的离子的鉴定方法:____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】端炔烃在催化剂存在下可发生偶联反应,称为Glaser反应。
![]()
该反应在研究新型发光材料、超分子化学等方面具有重要价值。如图是用利用Glaser反应制备化合物E的一种合成路线:
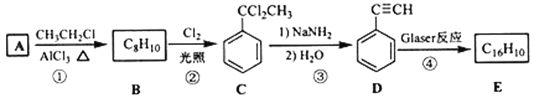
回答下列问题:
(1)B的化学名称为______________________________。
(2)③的反应类型为_________________________________。
(3)E的结构简式为__________________________________________________。用1 mol E合成1,4-二苯基丁烷,理论上需要消耗氢气________________________________mol。
(4)化合物(![]() )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为____________________________________________________________________________________________________________。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为____________________________________________________________________________________________________________。
(5)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3:1,写出其中2种的结构简式_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食品店出售的冰淇淋是硬化油,它是以多种植物油为原料来制得的,其中发生的反应有( )
A. 水解反应 B. 加聚反应
C. 加成反应 D. 氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO和O2,且恰好使两容器内气体密度相同。打开活塞,使NO与O2充分反应.下列判断正确的是(不考虑NO2转化为N2O4)
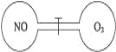
A.开始时左右两室分子数相同
B.反应前后NO室压强相同
C.最终容器内密度与原来相同
D.最终容器内无O2存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A,B,C,D的原子序数依次递增,它们的核电荷数之和为32,原子最外层电子数之和为10.A与C同主族,B与D同主族,A,C原子的最外层电子数之和等于B原子的次外层电子数.则下列叙述正确的是( )
A.D元素处于元素周期表中第3周期VIA族
B.四种元素的原子半径:A<B<C<D
C.B,D的最高价氧化物具有相似的物理性质和化学性质
D.一定条件下,B单质能置换出D单质,C单质能置换出A单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关气体摩尔体积的描述中正确的是( )。
A. 单位物质的量的气体所占的体积就是气体摩尔体积
B. 通常状况下,1摩尔气体的体积约为22.4L
C. 标准状况下的气体摩尔体积约为22.4L
D. 相同物质的量的气体摩尔体积也相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com