
£Ø8·Ö£©Ņ»¶ØĢõ¼žĻĀ£¬ŌŚĢå»żĪŖ3 LµÄĆܱÕČŻĘ÷ÖŠ£¬Ņ»Ńõ»ÆĢ¼ÓėĒāĘų·“Ӧɜ³É¼×“¼£Ø“߻ƼĮĪŖCu2O/ZnO£©£ŗCO(g)£«2H2(g) CH3OH(g)”£øł¾ŻĢāŅāĶź³ÉĻĀĮŠĪŹĢā£ŗ
CH3OH(g)”£øł¾ŻĢāŅāĶź³ÉĻĀĮŠĪŹĢā£ŗ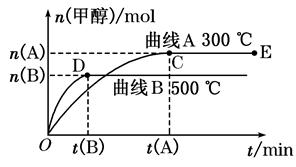
£Ø1£©·“Ó¦“ļµ½Ę½ŗāŹ±£¬Ę½ŗā³£Źż±ķ“ļŹ½K£½_________________£¬ÉżøßĪĀ¶Č£¬KÖµ___________£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©£¬Ę½ŗāĻņ ·½ĻņŅĘ¶Æ”£
£Ø2£©ŌŚ500”ę£¬“Ó·“Ó¦æŖŹ¼µ½Ę½ŗā£¬ĒāĘųµÄĘ½¾ł·“Ó¦ĖŁĀŹv(H2)£½________________”£
£Ø3£©ŌŚĘäĖūĢõ¼ž²»±äµÄĒéæöĻĀ£¬½«“¦ÓŚEµćµÄĢåĻµĢå»żŃ¹Ėõµ½ŌĄ“µÄ1/2£¬ĻĀĮŠÓŠ¹ŲøĆĢåĻµµÄĖµ·ØÕżČ·µÄŹĒ________£ØŃ”ĢīŃ”Ļī×ÖÄø£©”£
| A£®ĒāĘųµÄÅØ¶Č¼õÉŁ |
| B£®Õż·“Ó¦ĖŁĀŹ¼Óæģ£¬Äę·“Ó¦ĖŁĀŹŅ²¼Óæģ |
| C£®¼×“¼µÄĪļÖŹµÄĮæŌö¼Ó |
D£®ÖŲŠĀĘ½ŗāŹ±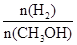 Ōö“ó Ōö“ó |
£Ø1£©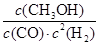 £» ¼õŠ” £» Äę·“Ó¦ £» £Ø2£©
£» ¼õŠ” £» Äę·“Ó¦ £» £Ø2£©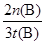 mol/(L”¤min) £»
mol/(L”¤min) £»
£Ø3£©BC £» £Ø4£©Cu2O£«CO 2Cu£«CO2
2Cu£«CO2
½āĪöŹŌĢā·ÖĪö£ŗ£Ø1£©»ÆŃ§Ę½ŗā³£ŹżŹĒŌŚŅ»¶ØĢõ¼žĻĀ£¬µ±æÉÄę·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬Éś³ÉĪļÅØ¶ČµÄĆŻÖ®»żŗĶ·“Ó¦ĪļÅØ¶ČµÄĆŻÖ®»żµÄ±ČÖµ£¬ĖłŅŌøł¾Ż·“Ó¦µÄ»Æѧ·½³ĢŹ½æÉÖŖ£¬øĆ·“Ó¦µÄĘ½ŗā³£ŹżK£½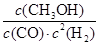 £»øł¾ŻĶ¼ĻńæÉÖŖ£¬ÉżøßĪĀ¶Č£¬¼×“¼µÄĪļÖŹµÄĮæ¼õŠ”£¬ÕāĖµĆ÷Ę½ŗāÄęĻņŅĘ¶Æ£¬Ņņ“Ė»ÆŃ§Ę½ŗā³£Źż¼õŠ””£
£»øł¾ŻĶ¼ĻńæÉÖŖ£¬ÉżøßĪĀ¶Č£¬¼×“¼µÄĪļÖŹµÄĮæ¼õŠ”£¬ÕāĖµĆ÷Ę½ŗāÄęĻņŅĘ¶Æ£¬Ņņ“Ė»ÆŃ§Ę½ŗā³£Źż¼õŠ””£
£Ø2£©ÓÉĶ¼ĻóæÉÖŖ£¬ŌŚ500”ꏱ£¬Ź±¼ä“ļµ½t(B)Ź±£¬¼×“¼µÄĪļÖŹµÄĮæĪŖn(B)£¬ĘäÅØ¶ČŹĒ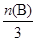 mol/L£¬Ōņøł¾Ż·½³ĢŹ½æÉÖŖ£¬ĻūŗÄĒāĘųµÄĪļÖŹµÄĮæÅØ¶ČŹĒ2”Į
mol/L£¬Ōņøł¾Ż·½³ĢŹ½æÉÖŖ£¬ĻūŗÄĒāĘųµÄĪļÖŹµÄĮæÅØ¶ČŹĒ2”Į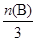 mol/L£¬ĖłŅŌŌŚ500”ę£¬“Ó·“Ó¦æŖŹ¼µ½Ę½ŗā£¬ĒāĘųµÄĘ½¾ł·“Ó¦ĖŁĀŹv(H2)£½
mol/L£¬ĖłŅŌŌŚ500”ę£¬“Ó·“Ó¦æŖŹ¼µ½Ę½ŗā£¬ĒāĘųµÄĘ½¾ł·“Ó¦ĖŁĀŹv(H2)£½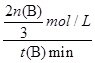 £½
£½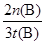 mol?£ØL?min£©-1”£
mol?£ØL?min£©-1”£
£Ø3£©ĘäĖūĢõ¼ž²»±äŹ±£¬½«“¦ÓŚEµćµÄĢåĻµĢå»żŃ¹Ėõµ½ŌĄ“µÄ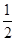 £¬ČŻĘ÷µÄĢå»ż¼õŠ”£¬ŌņŃ¹ĒæŌö“ó£¬ÕżÄę·“Ó¦ĖŁĀŹ¶¼Ōö“ó.ÓÉÓŚÕż·½Ó¦ŹĒĢå»ż¼õŠ”µÄ£¬ĖłŅŌĘ½ŗāĻņÕżĻņŅĘ¶Æ£¬¼×“¼µÄĪļÖŹµÄĮæŌö¶ą£¬ĒāĘųµÄĪļÖŹµÄĮæ¼õŠ”£¬µ«ÓÉÓŚĢå»ż¼õŠ”£¬Ę½ŗāŹ±ĒāĘųµÄÅØ¶Č·“¶ųŌö“ó£¬Ņņ“ĖÕżČ·“š°øŃ”BC”£
£¬ČŻĘ÷µÄĢå»ż¼õŠ”£¬ŌņŃ¹ĒæŌö“ó£¬ÕżÄę·“Ó¦ĖŁĀŹ¶¼Ōö“ó.ÓÉÓŚÕż·½Ó¦ŹĒĢå»ż¼õŠ”µÄ£¬ĖłŅŌĘ½ŗāĻņÕżĻņŅĘ¶Æ£¬¼×“¼µÄĪļÖŹµÄĮæŌö¶ą£¬ĒāĘųµÄĪļÖŹµÄĮæ¼õŠ”£¬µ«ÓÉÓŚĢå»ż¼õŠ”£¬Ę½ŗāŹ±ĒāĘųµÄÅØ¶Č·“¶ųŌö“ó£¬Ņņ“ĖÕżČ·“š°øŃ”BC”£
£Ø4£©ÓÉÓŚCOÄÜŗĶŃõ»ÆŃĒĶ·“Ó¦Cu2O+CO 2Cu+CO2£¬ĖłŅŌ¼ÓČė¶žŃõ»ÆĢ¼Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬ÓŠĄūÓŚŅÖÖĘ·“Ó¦ĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬Ī¬³ÖCu2OµÄĮæ²»±ä”£
2Cu+CO2£¬ĖłŅŌ¼ÓČė¶žŃõ»ÆĢ¼Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬ÓŠĄūÓŚŅÖÖĘ·“Ó¦ĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬Ī¬³ÖCu2OµÄĮæ²»±ä”£
æ¼µć£ŗæ¼²éĘ½ŗā³£Źż”¢Ķā½ēĢõ¼ž¶ŌĘ½ŗāדĢ¬µÄÓ°ĻģŅŌ¼°·“Ó¦ĖŁĀŹµÄ¼ĘĖćµČ



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
Ņ»¶ØĪĀ¶ČĻĀ2LµÄŗćČŻČŻĘ÷¼×ÖŠ£¬¼ÓČė2moLĢ¼ŗĶ2moLCO2·¢ÉśČēĻĀ·“Ó¦£ŗ C(s)+CO2(g)  2CO(g)”””÷H£¾0
2CO(g)”””÷H£¾0
²āµĆČŻĘ÷ÖŠCO2µÄĪļÖŹµÄĮæĖꏱ¼ätµÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾”£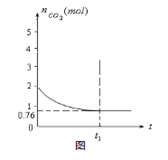
£Ø1£©øĆ·“Ó¦µÄ¦¤S”””” 0£ØĢī”°£¾”±”¢”°£¼”±»ņ”°£½”±£©”£ŌŚ”””” £ØĢī”°½Ļøß”±»ņ”°½ĻµĶ”±£© ĪĀ¶ČĻĀÓŠĄūÓŚøĆ·“Ó¦×Ō·¢½ųŠŠ”£
£Ø2£©ĮŠŹ½²¢¼ĘĖćÉĻŹöĪĀ¶ČĻĀ“Ė·“Ó¦µÄĘ½ŗā³£ŹżK”””””””” ”””””””” ”££Ø½į¹ū±£ĮōŅ»Ī»Š”Źż£©
£Ø3£©ĻņÉĻŹöĘ½ŗāĢåĻµÖŠŌŁĶØČėCO2£¬ŌņCO2µÄ×Ŗ»ÆĀŹ”””””” £ØĢīŌö“󔢼õŠ””¢²»±ä”¢ĪŽ·ØČ·¶Ø£©”£
£Ø4£©ĻąĶ¬ĪĀ¶ČĻĀ£¬2LµÄŗćČŻČŻĘ÷±ūÖŠ¼ÓČė4moLĢ¼”¢4moLCO2ŗĶ4moLCO”£æŖŹ¼·“Ó¦Ź±v(Õż)”””””””” v(Äę)£ØĢī£¾”¢ £¼”¢©£©”£
£Ø5£©ĻąĶ¬ĪĀ¶ČĻĀ£¬2LµÄŗćČŻČŻĘ÷ŅŅÖŠ¼ÓČė4moLĢ¼ŗĶ4moLCO2£¬“ļµ½Ę½ŗā”£ĒėŌŚĶ¼ÖŠ»³öŅŅČŻĘ÷ÖŠCO2µÄĪļÖŹµÄĮæĖꏱ¼ät±ä»Æ¹ŲĻµµÄŌ¤ĘŚ½į¹ūŹ¾ŅāĶ¼”££Ø×¢Ć÷Ę½ŗāŹ±CO2µÄĪļÖŹµÄĮ棩
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ĻĀĮŠĶ¼ĻóŌŚt1Ź±Ėł¶ŌÓ¦µÄ·“Ó¦Ģõ¼žøıäæÉÄÜĪŖ£ŗ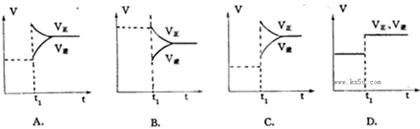
£Ø1£©ÉżøßĪĀ¶Č £¬£Ø2£©Ź¹ÓĆ“ß»Æ¼Į £¬
£Ø3£©Ōö“ó·“Ó¦ĪļÅØ¶Č £¬£Ø4£©¼õÉŁÉś³ÉĪļÅØ¶Č ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ÓŠĮ½øöĆܱÕČŻĘ÷AŗĶB£¬AČŻĘ÷ÖŠÓŠŅ»øöŅĘ¶ÆµÄ»īČūÄÜŹ¹ČŻĘ÷ÄŚ±£³ÖŗćŃ¹£¬BČŻĘ÷Äܱ£³ÖŗćČŻ”£ĘšŹ¼Ź±ĻņÕāĮ½øöČŻĘ÷ÖŠ·Ö±š³äČėµČĮæµÄĢå»ż±ČĪŖ2:lµÄSO2ŗĶO2µÄ»ģŗĻĘųĢ壬²¢Ź¹AŗĶBČŻ»żĻąµČ(ČēĶ¼ĖłŹ¾)£¬ŌŚ±£³Ö400”ęµÄĪĀ¶ČĻĀŹ¹Ö®·¢ÉśČēĻĀ·“Ó¦£ŗ2SO2+O2 2SO3”£ĢīŠ“ĻĀĮŠæÕ°×£ŗ
2SO3”£ĢīŠ“ĻĀĮŠæÕ°×£ŗ
(1)SO2µÄ×Ŗ»ÆĀŹ¦Į(A) ¦Į(B)”£(Ģī”°£¼”±”¢”°£¾”±»ņ”°=”±)
(2)“ļµ½(1)ĖłŹöĘ½ŗāŹ±£¬ČōĻņĮ½ČŻĘ÷ÖŠĶØČėÉŁĮæµÄė²Ęų£¬AČŻĘ÷»ÆŃ§Ę½ŗā ŅĘ¶Æ”£(Ģī”°ÕżĻņ”±”¢”°ÄęĻņ”±»ņ”°²»”±)
(3)“ļµ½(1)Ę½ŗāŗó£¬ĻņČŻĘ÷ÖŠ³äČėµČĮæµÄŌ·“Ó¦ĘųĢ壬ŌŁ“Ī“ļµ½Ę½ŗāŗó£¬BČŻĘ÷ÖŠSO3ŌŚ»ģŗĻĘųĢåÖŠµÄĢå»ż·ÖŹż ”£(Ģī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
£Ø16·Ö£©¹¤ŅµÉĻæÉŅŌŌŚŗćČŻĆܱÕČŻĘ÷ÖŠ²ÉÓĆĻĀĮŠ·“Ó¦Öʱø¼×“¼£ŗ
CO£Øg£©£«2H2£Øg£© CH3OH£Øg£©
CH3OH£Øg£©
£Ø1£©ĻĀĮŠĒéæöæÉŅŌ×÷ĪŖÅŠ¶Ļ·“Ó¦“ļµ½Ę½ŗāדĢ¬µÄŅĄ¾ŻµÄŹĒ£ØĢīŠņŗÅ£© ”£
A£®Éś³ÉCH3OH µÄĖŁĀŹÓėĻūŗÄH2µÄĖŁĀŹÖ®±ČĪŖ1©U2
B£®»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ±£³Ö²»±ä
C£®»ģŗĻĘųĢåµÄĆܶȱ£³Ö²»±ä
D£®ĢåĻµÄŚµÄŃ¹Ēæ±£³Ö²»±ä
£Ø2£©ĻĀ±ķĖłĮŠŹż¾ŻĪŖøĆ·“Ó¦ŌŚ²»Ķ¬ĪĀ¶ČĻĀµÄ»ÆŃ§Ę½ŗā³£Źż£ŗ
| ĪĀ¶Č/”ę | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |
| ČŻĘ÷ | ¼× | ŅŅ | ±ū | |
| Ķ¶ĮĻ·½Ź½ | 1molCO”¢2molH2 | 1molCH3OH | 2molCH3OH | |
| Ę½ŗāŹż¾Ż | C(CH3OH)/(mol/L) | c1 | c2 | c3 |
| ĢåĻµŃ¹Ēæ(Pa) | p1 | p2 | p3 | |
| ·“Ó¦µÄÄÜĮæ±ä»Æ | akJ | bkJ | ckJ | |
| ŌĮĻ×Ŗ»ÆĀŹ | ¦Į1 | ¦Į2 | ¦Į3 | |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ÖŠ¹śÄņĖŲŗĻ³ÉĖž(ÄņĖž)Ź¹ÓĆŹŁĆü½öĪŖÅ·ĆĄ¹ś¼ŅµÄ1/4”£ĪŖ“Ė±±¾©øÖĢśŃŠ¾æ Ōŗ¶ŌĖÄ“ØćņĢģ»ÆÄņĖžøÆŹ“¹ż³Ģ½ųŠŠŃŠ¾æ£¬µĆ³öĻĀĮŠøÆŹ“»śĄķ£ŗ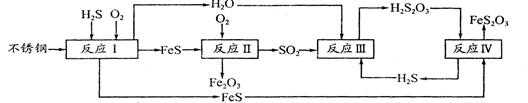
(1)H2SĄ“×ŌŗĻ³ÉÄņĖŲµÄĢģČ»Ęų”£ŌŚ380 K”¢Ģå»żĪŖ2 LµÄĆܱÕČŻĘ÷ÖŠ£¬“ęŌŚČēĻĀ·“Ó¦£ŗH2(g)£«S(s) H2S(g) ”÷H=£«21£®6kJ”¤mol£1”£·“Ó¦“ļµ½Ę½ŗāŹ±H2”¢S”¢H2SµÄĪļÖŹµÄĮæ¾łĪŖ3 mol£¬Ōņ380 KŹ±øĆ·“Ó¦µÄ»ÆŃ§Ę½ŗā³£ŹżĪŖ______£»ĻĀĮŠ¶ŌøĆ·“Ó¦·ÖĪöÕżČ·µÄŹĒ______(Ģī×ÖÄøŠņŗÅ)”£
H2S(g) ”÷H=£«21£®6kJ”¤mol£1”£·“Ó¦“ļµ½Ę½ŗāŹ±H2”¢S”¢H2SµÄĪļÖŹµÄĮæ¾łĪŖ3 mol£¬Ōņ380 KŹ±øĆ·“Ó¦µÄ»ÆŃ§Ę½ŗā³£ŹżĪŖ______£»ĻĀĮŠ¶ŌøĆ·“Ó¦·ÖĪöÕżČ·µÄŹĒ______(Ģī×ÖÄøŠņŗÅ)”£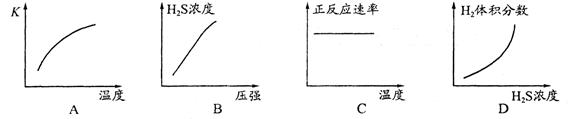
(2)ŌŚ·“Ó¦IÖŠ·¢ÉśµÄ»Æѧ·“Ó¦ĪŖ______”£
(3)ŃŠ¾æ·¢ĻÖ·“Ó¦IIŹĒ·Ö±šŅŌFe”¢FeSĪŖµē¼«£¬ŅŌĖ®Ä¤ĪŖµē½āÖŹČÜŅŗµÄµē»ÆѧøÆŹ“£¬Ęä øŗ
¼«ĪŖ______£»
ŅŃÖŖ£ŗFe(s)£«S(s)=FeS(s) ”÷H1=£2£®5akJ”¤mol£1
S(s)£«O2(g)=SO2(g) ”÷H2=£5akJ”¤mol£1
4Fe(s)£«3O2(g)=2Fe2O3(s) ”÷H3=£6akJ”¤mol£1
Ōņ·“Ó¦IIµÄČČ»Æѧ·½³ĢŹ½ĪŖ_____
(4)ŅŃÖŖH2S2O3µÄK1=2£®2”Į10-1”¢K2=2£®8”Į10-2”£Na2S2O3Ė®ČÜŅŗ³Ź______ŠŌ£¬øĆČÜŅŗÖŠµēŗÉŹŲŗćŹ½ĪŖ_____ £»·“Ó¦IYµÄ·“Ó¦ĄąŠĶĪŖ______ £»øĆ·“Ó¦______(Ģī”°ÄÜ”±»ņ”°²»ÄÜ”±£© ĖµĆ÷FeSČܽāŠŌĒæÓŚFeS2O3
(5)ćņĢģ»ÆÄņĖžµÄ×īÖÕøÆŹ“²śĪļĪŖ______£»ĪŖĮĖÓŠŠ§·ĄøÆ£¬±±øÖ½ØŅéćņĢģ»ÆŌŚÉś²śÖŠÓĆ CuSO4ČÜŅŗ”°ĶŃĮņ(H2S)”±£¬ĘäÖŠÉę¼°µÄĄė×Ó·½³ĢŹ½ĪŖ
__________________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
I£®Éč·“Ó¦¢ŁFe(s)+CO2(g) FeO(s)+CO(g)µÄĘ½ŗā³£ŹżĪŖK1”£·“Ó¦ ¢ŚFe(s)+H2O(g)
FeO(s)+CO(g)µÄĘ½ŗā³£ŹżĪŖK1”£·“Ó¦ ¢ŚFe(s)+H2O(g)  FeO(s)+H2(g)µÄĘ½ŗā³£ŹżĪŖK2£¬ŌŚ²»Ķ¬ĪĀ¶ČĻĀ£¬K1”¢K2µÄÖµČēĻĀ£ŗ
FeO(s)+H2(g)µÄĘ½ŗā³£ŹżĪŖK2£¬ŌŚ²»Ķ¬ĪĀ¶ČĻĀ£¬K1”¢K2µÄÖµČēĻĀ£ŗ
| T(K) | K1 | K2 |
| 973 | 1.47 | 2.36 |
| 1173 | 2.15 | 1.67 |
 CO(g)+H2O(g)£¬ÕāŹĒŅ»øö (Ģī”°Īü”±»ņ”°·Å”±)ČČ·“Ó¦£¬ŅŖŹ¹Ę½ŗā¢ŪĻņÓŅŅĘ¶Æ£¬æɲÉČ”µÄ“ėŹ©ÓŠ (ĢīŠņŗÅ)”£
CO(g)+H2O(g)£¬ÕāŹĒŅ»øö (Ģī”°Īü”±»ņ”°·Å”±)ČČ·“Ó¦£¬ŅŖŹ¹Ę½ŗā¢ŪĻņÓŅŅĘ¶Æ£¬æɲÉČ”µÄ“ėŹ©ÓŠ (ĢīŠņŗÅ)”£ FeO(s)+CO(g)ŌŚĪĀ¶ČT1ĻĀ½ųŠŠ£»Fe(s)+H2O(g)
FeO(s)+CO(g)ŌŚĪĀ¶ČT1ĻĀ½ųŠŠ£»Fe(s)+H2O(g)  FeO(s)+H2(g)ŌŚĪĀ¶ČT2ĻĀ½ųŠŠ£¬ŅŃÖŖT1£¾T2£¬ĒŅc(CO2)£¾c(H2O)(ĘäĖūĢõ¼ž¾łĻąĶ¬)£¬ŌņĮ½Õߵķ“Ó¦ĖŁĀŹ (ĢīŠņŗÅ)”£
FeO(s)+H2(g)ŌŚĪĀ¶ČT2ĻĀ½ųŠŠ£¬ŅŃÖŖT1£¾T2£¬ĒŅc(CO2)£¾c(H2O)(ĘäĖūĢõ¼ž¾łĻąĶ¬)£¬ŌņĮ½Õߵķ“Ó¦ĖŁĀŹ (ĢīŠņŗÅ)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
Cl2ŗĻ³ÉÓŠ»śĪļŹ±»į²śÉśø±²śĪļHC1”£4HCl+O2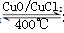 2Cl2+2H2O£¬æÉŹµĻÖĀȵÄŃ»·ĄūÓĆ”£
2Cl2+2H2O£¬æÉŹµĻÖĀȵÄŃ»·ĄūÓĆ”£
Ķź³ÉĻĀĮŠĢīæÕ£ŗ
£Ø1£©øĆ·“Ó¦Ę½ŗā³£ŹżµÄ±ķ“ļŹ½K= £»Čō·“ӦȯĘ÷µÄČŻ»żĪŖ2L£¬8minŗó“ļµ½Ę½ŗā£¬²āµĆČŻĘ÷ÄŚĪļÖŹÓÉ2.5mol¼õÉŁÖĮ2.25mol£¬ŌņHClµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ mol/L? min”£
£Ø2£©ČōøĆ·“Ó¦ŌŚĢå»ż²»±äµÄĆܱÕČŻĘ÷ÖŠ·¢Éś£¬µ±·“Ó¦“ļĘ½ŗāŹ±£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ ”£
a£®v (HCl)="2" v(Cl2)
b£®4vÕż(HCl)= vÄę(O2)
c£®ÓÖ¼ÓČė1mol O2£¬“ļŠĀĘ½ŗāŹ±£¬HClµÄ×Ŗ»ÆĀŹŌö“ó
d£®·ÖĄė³öH2O£¬“ļŠĀĘ½ŗāŹ±£¬vÕż(HCl)Ōö“ó
£Ø3£©ĻĀĶ¼ŹĒøĆ·“Ó¦Į½ÖÖĶ¶ĮĻ±Č[n (HCl):n (O2)·Ö±šĪŖ4:1ŗĶ2:1 ] ĻĀ£¬·“Ó¦ĪĀ¶Č¶ŌHClĘ½ŗā×Ŗ»ÆĀŹÓ°ĻģµÄĒśĻß”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ ”£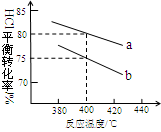
a£®øĆ·“Ó¦µÄÕż·“Ó¦ŹĒ·ÅČČ·“Ó¦
b£®ĘäĖūĢõ¼ž²»±ä£¬ÉżøßĪĀ¶Č£¬Ę½ŗā³£ŹżKÖµŌö“ó
c£®ČōĘ½ŗā³£ŹżKÖµ±ä“󣬓ļŠĀĘ½ŗāĒ°vÄęŹ¼ÖÕ¼õŠ”
d£®ČōĘ½ŗā³£ŹżKÖµ±ä“ó£¬ŌņĘ½ŗāĻņÕż·“Ó¦·½ĻņŅʶÆ
£Ø4£©Ķ¶ĮĻ±ČĪŖ4:1”¢ĪĀ¶ČĪŖ400”ꏱ£¬Ę½ŗā»ģŗĻĪļÖŠCl2µÄĪļÖŹµÄĮæ·ÖŹżŹĒ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ŌŚŅ»øö¹Ģ¶ØĢå»żµÄĆܱÕČŻĘ÷ÖŠ£¬ĻņČŻĘ÷ÖŠ³äČė2 mol A ŗĶ1 mol B£¬·¢ÉśČēĻĀ·“Ó¦£ŗ2A(g) £« B(g)  3C(g) £« D(s)£¬·“Ó¦“ļµ½Ę½ŗāŹ±CµÄÅضČĪŖ1.2 mol/L.
3C(g) £« D(s)£¬·“Ó¦“ļµ½Ę½ŗāŹ±CµÄÅضČĪŖ1.2 mol/L.
£Ø1£©ČōŹ¹ČŻĘ÷ĪĀ¶ČÉżøߣ¬Ę½ŗāŹ±»ģŗĻĘųĢåµÄĘ½¾łĻą¶ŌĦ¶ūÖŹĮæ¼õŠ”£¬ŌņÕż·“Ó¦ĪŖ________£ØĢī”°ĪüČČ”±»ņ”°·ÅČČ”±£©·“Ó¦£®
£Ø2£©ČōĪ¬³ÖČŻĘ÷Ģå»żŗĶĪĀ¶Č²»±ä£¬°“ĻĀĮŠ·½·Ø¼ÓČėĘšŹ¼ĪļÖŹ£¬“ļµ½Ę½ŗāŹ±CµÄÅضČČŌĪŖ1.2 mol/LµÄŹĒ______£ØÓĆŠņŗÅĢīæÕ£©£®
¢Ł4 mol A£«2 mol B””¢Ś3 mol C£«1 mol D£«l mol B
¢Ū3 mol C£«2 mol D””¢Ü1.6 mol A£«0.8 mol B£«0.6 mol C
£Ø3£©Ä³ĪĀ¶ČĻĀ£¬ĻņČŻĘ÷ÖŠ¼ÓČė3 mol CŗĶ0.8 mol D£¬·“Ó¦“ļµ½Ę½ŗāŹ±CµÄÅضČČŌĪŖ1.2 mol/L£¬ŌņČŻĘ÷µÄČŻ»żVÓ¦“óÓŚ________L£¬Š”ÓŚ________L.
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com