
【题目】人体血液里Ca2+的浓度一般采用mg·cm-3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用酸性KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度。
I.(配制酸性KMnO4标准溶液)如图是配制50 mL酸性KMnO4标准溶液的过程示意图。

(1)请你观察图示判断其中不正确的操作有____(填序号)。
(2)其中确定50 mL溶液体积的容器是____(填名称)。
(3)如果按照图示的操作所配制的溶液进行实验,在其他操作均正确的情况下,所测的实验结果将_______(填“偏大”或“偏小”)。
II.(测定血液样品中Ca2+的浓度)抽取血样20. 00 mL,经过上述处理后得到草酸,再用0.020 mol/L酸性KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00 mL酸性KMnO4溶液。
(4)已知草酸与酸性KMn04溶液反应的离子方程式为:5H2C2O4+2MnO4-+6H+=2Mnx++10CO2↑+8H2O,则式中的x=____。
(5)滴定时,根据现象____,即可确定反应达到终点。
(6)经过计算,血液样品中Ca2+的浓度为____mg.cm-3。
【答案】②⑤ 50mL容量瓶 偏小 2 溶液由无色变为紫红色,且半分钟内不褪色 1.2
【解析】
(1)根据配制一定物质的量浓度的溶液的正确操作结合图示分析;
(2)容量瓶是确定溶液体积的仪器;
(3)仰视刻度线,会使溶液体积偏大,结合C=n/V分析;
(4)草酸跟酸性KMnO4溶液反应生成二氧化碳、二价锰离子等,结合氧化还原反应得失电子守恒和根据电荷守恒进行分析,写出化学方程式得到x;
(5)滴定时,用高锰酸钾滴定草酸,反应达到终点时,滴入的高锰酸钾溶液不褪色,据此判断;
(6)根据滴定数据及钙离子与高锰酸钾的关系式计算出血液样品中Ca2+的浓度.
(1)由图示可知②⑤操作不正确,②不能在量筒中溶解固体,⑤定容时应平视刻度线,至溶液凹液面与刻度线相切;
(2)应该用容量瓶准确确定50mL溶液的体积;
(3)用图示的操作配制溶液,仰视刻度线,会使溶液体积偏大,所配制的溶液浓度将偏小;
(4)根据电荷守恒,(-1×2)+(+1×6)=+x×2,解得,x=2,草酸跟KMnO4反应的离子方程式为:2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O;
(5)滴定时,用高锰酸钾滴定草酸,反应达到终点时的现象为溶液由无色变为紫红色,且半分钟内不褪色;
(6)血样20.00mL经过上述处理后得到草酸,草酸消耗的消耗的高锰酸钾的物质的量为:0.020mol·L-1×0.012L=2.4×10-4mol,根据反应方程式2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O,及草酸钙的化学式CaC2O4,可知:n(Ca2+)=n(H2C2O4)=5/2n(MnO4-)=2.5×2.4×10-4mol=6×10-4mol,Ca2+的质量为:40g·mol-1×6×10-4mol=0.024g,钙离子的浓度为:0.024g/20cm 3=1.2 mg·cm-3。


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
【题目】下列推断合理的是( )
A. 某无色溶液中加入Ba(NO3)2溶液,再加入盐酸,沉淀不溶解,则原溶液中一定有SO42-
B. 单质![]() 氧化物
氧化物![]() 酸或碱
酸或碱![]() 盐,能按照上述转化关系直接转化的可以是硫元素
盐,能按照上述转化关系直接转化的可以是硫元素
C. 浓硫酸有强氧化性,常温下能与Cu发生剧烈反应
D. 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成,该溶液中一定含有SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列说法正确的是
A. 常温常压下,124 g P4中所含P—P键数目为4NA
B. 100 mL 1mol·L1FeCl3溶液中所含Fe3+的数目为0.1NA
C. 标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA
D. 密闭容器中,2 mol SO2和1 mol O2催化反应后分子总数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某学习小组用下图装置测定铝镁合金中铝的质量分数和铝的相对原子质量。
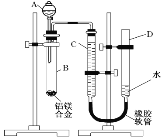
(1)实验前,先将铝镁合金在稀酸中浸泡片刻。检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:
①记录C的液面位置;②待B中不再有气体产生并恢复至室温后,记录C的液面位置;③检查气密性;④由A向B中滴加足量试剂;⑤将B中剩余固体过滤,洗涤,干燥,称重,上述操作的顺序是_______,(填序号)②中记录C的液面位置前,还应______。
(2)A中装的试剂为________。
(3)若实验用铝镁合金的质量为m1g,测得氢气体积为amL(已换算为标准状况),B中剩余固体的质量为m2g,则铝的相对原子质量为_______。
II.某化学研究小组的同学,为了探究催化剂对化学反应速率的影响,做了以下实验:将0.20mol MnO2粉末加入50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示
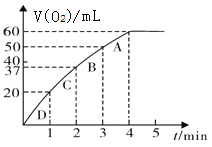
(4)A、B、C、D各点反应速率快慢的顺序为_______。
(5)计算H2O2的初始物质的量浓度_____ (请保留两位有效数字) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自来水常用二氧化氯(ClO2)来杀菌消毒,它能转化为可溶性氯化物,市场上有些不法商贩为牟取暴利,用自来水冒充纯净水出售,为辨别纯净水的真伪,你想选用的化学试剂是( )
A.氯化钡溶液B.石蕊试液C.硝酸银溶液D.氢氧化钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是( )
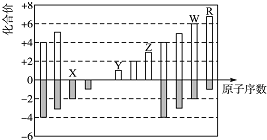
A. 原子半径:X<Y<Z
B. 气态氢化物的稳定性及其水溶液的酸性:R>W
C. W、X形成的化合物以及它们与水反应生成物都是共价化合物
D. Y、Z、W的最高价氧化物对应的水化物两两之间都能发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某芳香烃A分子式为C8H10,它的主要用途是在石油化学工业作为生产苯乙烯的中间体,所制成的苯乙烯一般被用来制备常用的塑料制品——聚苯乙烯。某烃类衍生物X,分子式为C15H14O3,能使FeCl3溶液显紫色。J分子内有两个互为对位的取代基。在一定条件下各物质间有如下的转化关系:(无机物略去)

(1)A物质的名称为__________。写出核磁共振氢谱中只有2个特征峰的A的同分异构体的结构简式__________________。
(2)写出X的结构简式______________;J中所含的含氧官能团的名称为_________。
(3)E与H反应的化学方程式是_______________;反应类型是______________。
(4)B、C的混合物在NaOH 乙醇溶液中加热可以生成同一种有机物I,以I为单体合成的高分子化合物的结构简式是_________________。
(5)已知J有多种同分异构体,写出一种符合下列性质的J的同分异构体的结构简式________。
①与FeCl3溶液作用显紫色;②与新制Cu(OH)2悬浊液作用产生红色沉淀;
③苯环上的一卤代物有2种;④能发生水解反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有①Na2S、②金刚石、③NH4Cl、④Na2SO4、⑤干冰、⑥碘片六种物质,按下列要求回答:
(1)熔化时不需要破坏化学键的是____________,熔化时需要破坏共价键的是____________,熔点最高的是____________,熔点最低的是_____________(填序号)。
(2)属于离子化合物的是_______________________,只有离子键的物质是____________,以分子间作用力结合的物质是____________________(均填序号),③的电子式____________________。
(3)用电子式表示①的形成过程是______________________,用电子式表示⑥的形成过程是_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com