
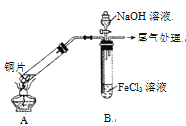
【题目】某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如右图所示(夹持仪器已略去)。
(1)实验前,应先检查装置的 ;实验中产生的尾气应通入 溶液进行处理。
(2)实验过程中需要配制100 mL l mo1·L-1 FeCl3溶液,所需要的玻璃仪器有:烧杯、量筒、玻璃棒、 ;实际配制过程中,常先将FeCl3固体完全溶于适量稀盐酸中,再加水稀释,此特殊操作的目的是____。
(3)该小组同学向5 mL l mo1·L-1 FeCl3溶液中通入足量的SO2,溶液最终呈浅绿色,写出其反应的离子方程式 。再打开分液漏斗活塞,逐滴加入煮沸冷却后的NaOH稀溶液,则试管B中产生的实验现象是 。
(4)该小组同学在(3)中实验时,发现溶液变为浅绿色需要较长时间,在此期间同学们观察到的现象是溶液由棕黄色变成红棕色,没有观察到丁达尔效应,最终溶液呈浅绿色。
【查阅资料】Fe(HSO3)2+在溶液中呈红棕色且具有较强的还原性,能被Fe3+氧化为SO42-。则Fe(HSO3)2+与Fe3+在溶液中反应的离子方程式是 。
(5)若实验中用5 mL一定浓度的浓H2SO4与适量Cu片充分反应,实验结束后,测得产生SO2的体积在标准状况下为672 mL,向已冷却的A试管溶液中加入4 mo1·L-1的NaOH溶液30 mL时,恰好使Cu2+完全沉淀。则所用浓H2SO4浓度为____。(忽略过程中溶液的体积变化)
【答案】(1)气密性; NaOH;(2)100 mL容量瓶、胶头滴管;抑制FeCl3水解;(3)2Fe3++SO2+2H2O=2Fe2++SO42-+4H+;先无现象,后生成白色絮状沉淀;(4)Fe(HSO3)2++Fe3++H2O=2Fe2++SO42-+3H+;(5)18 mo1·L-1.
【解析】
试题分析:(1)实验前,应先检查装置的气密性;实验中产生的尾气是SO2,应通入NaOH溶液进行处理;(2)实验过程中需要配制100 mL l mo1·L-1 FeCl3溶液,配制一定物质的量浓度的溶液需要的玻璃仪器有:烧杯、量筒、玻璃棒、100mL容量瓶、定容时还要用到胶头滴管,配制过程中,由于Fe3+容易发生水解,常先将FeCl3固体完全溶于适量稀盐酸中,再加水稀释,抑制Fe3+的水解,答案为:100 mL容量瓶、胶头滴管;抑制FeCl3水解;(3)向5 mL l mo1·L-1 FeCl3溶液中通入足量的SO2,溶液最终呈浅绿色,生成了Fe2+,SO2被氧化为H2SO4,发生的离子方程式为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,试管中有硫酸和硫酸亚铁,加入稀NaOH溶液,先和硫酸发生中和反应,这一阶段无明显现象,当硫酸反应完后,将和硫酸亚铁反应生成氢氧化亚铁,由于氢氧化钠是煮沸除去了氧气的,所以氢氧化亚铁不会被氧化为氢氧化铁,答案为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+;先无现象,后生成白色絮状沉淀;(4)Fe(HSO3)2+在溶液中呈红棕色且具有较强的还原性,能被Fe3+氧化为SO42-,则Fe3+被还原为Fe2+,反应的离子方程式为:Fe(HSO3)2++Fe3++H2O=2Fe2++SO42-+3H+;(5)5 mL一定浓度的浓H2SO4与适量Cu片充分反应,实验结束后,测得产生SO2的体积在标准状况下为672 mL,Cu+2H2SO4=CuSO4+SO2↑+2H2O,n(SO2)=0.672L/22.4L/mol=0.03mol, 算出n(CuSO4)=0.03mol,n1(H2SO4)=0.06mol, 向已冷却的A试管溶液中加入4 mo1·L-1的NaOH溶液30 mL时,恰好使Cu2+完全沉淀,Cu不会和稀硫酸反应,A中还有稀硫酸,当加入NaOH溶液时,首先和未反应的硫酸反应,硫酸反应完后再和CuSO4反应,CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,
n1 (NaOH)=2n(CuSO4)=0.06mol,和硫酸反应的氢氧化钠的物质的量为n2(NaOH)=4mol·L-1×0.03L-0.06mol=0.06mol,n2(H2SO4)=0.06mol/2=0.03mol,总硫酸的物质的量为0.03mol+0.06mol=0.09mol,c(H2SO4)=0.09mol/0.005L=18mol/L,答案为:18mol/L.


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】表示溶液浓度的方法通常有两种:溶液中溶质的质量分数(w)和物质的量浓度(c),因此在配制溶液时,根据不同的需要,有不同的配制方法。请完成下列填空题。 (导学号52080091)
(1)用10%(密度为1.01 g·cm-3)的氢氧化钠溶液配制成27.5 g 2%的氢氧化钠溶液。
①计算:需____g 10%(密度为1.01 g·cm-3)的氢氧化钠溶液,其体积为___ mL,需加____ mL水[(水)=1 g·cm-3]进行稀释。
②量取:用____ mL量筒量取10%的氢氧化钠溶液,量取时视线要跟量筒内液体____相平,然后倒入烧杯里,用____ mL量筒量取蒸馏水注入烧杯里。
③溶解:用____将上述溶液搅拌均匀,即得27.5 g 2%的氢氧化钠溶液。
(2)把溶质质量分数为98%(密度为1.84 g·cm-3)的浓硫酸稀释成3 mol·L-1的稀硫酸100 mL。
①需要量取浓硫酸____mL;
②配制操作可分解成如下几步,正确的操作顺序是____________(填编号)。
A.向容量瓶中注入少量蒸馏水,检查是否漏水
B.用少量蒸馏水洗涤烧杯及玻璃棒,将溶液注入容量瓶中,并重复操作两次
C.把已冷却的稀硫酸注入经检查不漏水的容量瓶中
D.根据计算,用量筒量取一定体积的浓硫酸
E.将浓硫酸沿烧杯壁慢慢注入盛有蒸馏水的小烧杯中,并不断用玻璃棒搅拌
F.盖上容量瓶的塞子,振荡,摇匀
G.用胶头滴管滴加蒸馏水,使溶液凹液面最低处恰好与刻度线相切
H.继续往容量瓶中小心地加蒸馏水,使液面接近刻度线
(3)实验室需配制1 mol·L-1的NaOH溶液和1 mol·L-1的H2SO4溶液各100 mL。
①要配制NaOH溶液,在用托盘天平称取NaOH固体时,托盘天平读数为____(填编号,下同)。
A.4.0 g
B.小于4.0 g
C.大于4.0 g
②在配制NaOH溶液和H2SO4溶液的各步操作中,有明显不同的是____。
A.称量或量取 B.溶解
C.移液、洗涤 D.定容
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物种类繁多的主要原因是( )
A. 有机物的分子结构十分复杂
B. 碳原子能与其他原子形成四个共价键,而且碳原子之间也能互相成键
C. 有机物除含碳元素外,还含有其他多种元素
D. 自然界中存在多种形式的、大量的有机物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中化学键的类型完全相同的是( )
A. NH4Cl H2O CO2 B. NaCl MgCl2Na2O
C. H2O Na2O CO2 D. CaCl2 NaOH H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列氯化物中,既能由金属和氯气直接反应制得,又能由金属和盐酸反应制得的是
A. CuCl2 B. FeCl2 C. FeCl3 D. AlCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)基态原子变成激发态原子产生的光谱叫_______光谱。第四周期中基态原子的M层电子全满的元素位于周期表的_______区,其中未成对电子数为1的有_______种。
(2)已知液态二氧化硫可以发生类似于水的自身电离2SO2(l)![]() SO2++SO32-,SO2+中的σ键和π键数目比为_______,写出一种与SO2+互为等电子体的单质分子_______。
SO2++SO32-,SO2+中的σ键和π键数目比为_______,写出一种与SO2+互为等电子体的单质分子_______。
(3)氯化钠的晶胞如图所示,钠离子周围紧邻的氯离子形成的几何构型是_______。若钠离子和氯离子的半径分别是apm和bpm,则氯化钠晶体的空间利用率是_______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于碳骨架异构的是( )
A.CH3CH2CH2CH3和CH3CH(CH3)2
B.CH2=CHCH2CH3和CH3CH=CHCH3
C.顺-1,2-二氯乙烯和反-1,2-二氯乙烯
D.CH3CH2CH2COOH 和CH3COOCH2CH2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com