
��֪һ�������¶���1mol���л�ѧ����Ҫ���յ������ֱ�Ϊ��H���� 436 kJ��
Cl��Cl 243 kJ��H��Cl 431 kJ�����ڷ�Ӧ H2(g)+ Cl2 (g) =" 2HCl" (g)��
����˵����ȷ���ǣ� ��
| A���÷�Ӧ�ķ�Ӧ�� ?H �� 0 |
| B�����������еĻ�ѧ�������������еĻ�ѧ�����ȶ� |
| C����ͬ�����£��÷�Ӧ�ڹ��պ͵�ȼ�����µ�?H��ͬ |
| D��H2��Cl2��Ӧ���Ȼ�ѧ����ʽΪ H2(g) +Cl2(g) = 2HCl(g)?H =" -183" kJ |
B
���������������Ӧ�Ⱦ��Ƕϼ����յ��������γɻ�ѧ�����ų��������IJ�ֵ�����Ը��ݼ��ܿ�֪���÷�Ӧ�ķ�Ӧ���ǡ�H��436kJ/mol��243 kJ/mol��2��431 kJ/mol����183 kJ/mol��A����ȷ�����ݼ��ܴ�С���жϣ�ѡ��B��ȷ����Ӧ���뷴Ӧ������ϵ��C����ȷ��D����ȷ����Ӧ�ȵĵ�λ��kJ/mol����ѡB��
���㣺���鷴Ӧ�ȵ��й��ж�
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣��Ҫ�ǿ���ѧ���Է�Ӧ�ȸ������Ϥ���ճ̶ȣ�����������ѧ���Ļ���֪ʶ�����ѧ����Ӧ��������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪һ�������¶��ѻ�����ijЩ��ѧ���������仯�������ʾ��
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �����ڻ��ʡ���������л��ϳɹ�ҵ�ж��й㷺Ӧ�ã�
�����ڻ��ʡ���������л��ϳɹ�ҵ�ж��й㷺Ӧ�ã�
| ||
| ||
| ���� |
| ���¸�ѹ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
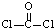 ����COCl2�����ں���
����COCl2�����ں����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�������г�����2012�������ѧ����ĩ���Ի�ѧ���� ���ͣ�013
|
��֪һ�������¶��ѻ�����ijЩ��ѧ����������ϵ���±���
���ڷ�Ӧ��H2(g)��Cl2(g)��2HCl(g)������˵����ȷ���� | |
| [����] | |
A�� |
�÷�Ӧ�ķ�Ӧ�Ȧ�H��0 |
B�� |
����1 mol��HC1ʱ��Ӧ����431 kJ |
C�� |
���������еĻ�ѧ�������������еĻ�ѧ�����ι� |
D�� |
��ͬ�����£��������Ӿ��е����������������Ӿ��е����� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com