
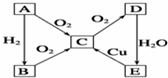
 已知,A为空气中含量最多的单质.根据如图转化关系,回答下列问题:
已知,A为空气中含量最多的单质.根据如图转化关系,回答下列问题:分析 A为空气中含量最多的单质,则A为N2,A与氧气反应生成C为NO,A与氢气反应生成B为NH3,C与氧气饭生成D为NO2,D与水反应生成B为HNO3,以此来解答.
解答 解:A为空气中含量最多的单质,则A为N2,A与氧气反应生成C为NO,A与氢气反应生成B为NH3,C与氧气饭生成D为NO2,D与水反应生成B为HNO3,
(1)由上述分析可知,A为N2,D为NO2,故答案为:N2;NO2;
(2)E→C的反应方程式为3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,故答案为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O;
(3)久置的E的浓溶液常常呈黄色,原因是硝酸分解生成的二氧化氮溶解在溶液中,故答案为:硝酸分解生成的二氧化氮溶解在溶液中.
点评 本题考查无机物的推断,为高频考点,把握含N物质之间的转化为解答的关键,侧重分析与推断能力的考查,注意A为氮气是物质推断的突破口,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 乙炔通入酸性高锰酸钾溶液中,溶液褪色 | |
| B. | 苯滴入溴水中,振荡后溴水层接近无色 | |
| C. | 油脂的皂化反应 | |
| D. | 将含裂化获得的汽油滴入溴水中,溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
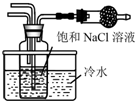
| A. | a 通入 CO2,然后 b 通入 NH3,c 中放碱石灰 | |
| B. | b 通入 NH3,然后 a 通入 CO2,c 中放碱石灰 | |
| C. | a 通入 NH3,然后 b 通入 CO2,c 中放蘸稀硫酸的脱脂棉 | |
| D. | b 通入 CO2,然后 a 通入 NH3,c 中放蘸稀硫酸的脱脂棉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纤维素和淀粉遇碘水均显蓝色 | |
| B. | 溴乙烷与NaOH乙醇溶液共热生成乙烯 | |
| C. | 蛋白质、乙酸和葡萄糖均属非电解质 | |
| D. | 乙酸乙酯和食用植物油均可水解生成乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | HClO4、H3PO4、H2SO4的酸性依次减弱 | |
| B. | HCl、HBr、HI的稳定性依次减弱 | |
| C. | N、O、F原子半径逐渐增大 | |
| D. | 钠、镁、铝的还原性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg(OH)2( Al(OH)3) | B. | MgCl2(AlCl3) | C. | Mg(Al) | D. | MgO(Al2O3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③①⑥⑦②④⑤ | B. | ⑥①②⑦③④⑤ | C. | ⑤④③①⑥⑦② | D. | ⑥③⑦①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用于计算烃完全燃烧时的耗氧量 | B. | 式中的m只可能是大于0的偶数 | ||
| C. | 式中的m不可能是小于n | D. | 所表示的反应一定是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 短周期元素a、b、c、d的原子序数依次增大.它们分属于不同主族,这四种元素的原子电子层数之和为8.A、B、C、D依次为a、b、c、d的单质,甲、乙、丙分子内原子数依次为4、3、2.在一定条件下可以发生如图所示的化合反应.
短周期元素a、b、c、d的原子序数依次增大.它们分属于不同主族,这四种元素的原子电子层数之和为8.A、B、C、D依次为a、b、c、d的单质,甲、乙、丙分子内原子数依次为4、3、2.在一定条件下可以发生如图所示的化合反应. ,若将甲通入乙中所得溶液PH大于7,用方程式表示溶液PH大于7 的原因:NH3•H2O?NH4++OH-.
,若将甲通入乙中所得溶液PH大于7,用方程式表示溶液PH大于7 的原因:NH3•H2O?NH4++OH-.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com