
| A. | pH相同的盐酸与氯化铵溶液中,水的电离程度相同 | |
| B. | 溶液加水稀释时,$\frac{c(N{H}_{3}{H}_{2}O)•c({H}^{+})}{c(N{H}_{4}^{+})}$逐渐增大 | |
| C. | 加入少量Mg(OH)2固体,c(NH4+)减小 | |
| D. | 加入等体积0.05mol﹒L-1NaOH溶液时:c(Na+)=c(CI-)>c(NH4+)>c(OH-)>c(H+) |
分析 A.酸抑制水的电离、能水解的盐促进水的电离;
B.水解常数只受温度影响;
C.NH4+能与Mg(OH)2电离的OH-结合生成NH3•H2O;
D.0.1mol•L-1的NH4Cl溶液中加入等体积0.05mol﹒L-1NaOH溶液,溶液中溶质为等浓度的NaCl、NH3•H2O、NH4Cl.
解答 解:A.酸抑制水的电离、能水解的盐促进水的电离,pH相同的盐酸与氯化铵溶液,氯化铵溶液中水的电离程度大于盐酸中水的电离程度,故A错误;
B.水解常数只受温度影响,溶液加水稀释时,水解常数Kh=$\frac{c(N{H}_{3}{H}_{2}O)•c({H}^{+})}{c(N{H}_{4}^{+})}$不变,故B错误;
C.0.1mol•L-1的NH4Cl溶液中加入少量Mg(OH)2固体,NH4+能与Mg(OH)2电离的OH-结合生成NH3•H2O,所以c(NH4+)减小,故C正确;
D.0.1mol•L-1的NH4Cl溶液中加入等体积0.05mol﹒L-1NaOH溶液,溶液中溶质为等浓度的NaCl、NH3•H2O、NH4Cl,溶液显碱性,溶液中离子浓度关系为c(NH4+)>c(Na+)=c(CI-)>c(OH-)>c(H+),故D错误.
故选C.
点评 本题考查盐类的水解、离子浓度大小比较,题目难度中等,试题侧重于影响盐类水解的因素的考查,有利于培养学生的良好的科学素养和提高学习的积极性,解题时结合影响盐类水解的因素分析.


科目:高中化学 来源:2016-2017学年重庆市高二上半期考试化学卷(解析版) 题型:选择题
下列说法正确的是
A.正反应是放热反应的可逆反应,升高温度v(正)>v(逆)
B.升高温度或使用催化剂是通过增加活化分子百分数而使反应速率加快
C.勒夏特列原理只使用于可逆反应,不使用于溶解和弱电解质的电离
D.△G=△H-T△S适合任意条件的化学反应进行的方向判据
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14g氮气含有的原子数为0.5NA | |
| B. | 4 g金属钙变成钙离子时失去的电子数为0.1NA | |
| C. | 1 mol O2分子的质量等于1 mol氧原子的质量 | |
| D. | 16 g O2分子和16g O3分子所含的氧原子数目相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、K+、Cl-、NO3- | B. | Cu2+、K+、SO42-、NO3- | ||
| C. | Na+、Ag+、NO3-、HCO3- | D. | Na+、NH4+、CO32-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.5 mol•L-1•s-1 | B. | v(B)=0.3 mol•L-1•s-1 | ||
| C. | v(C)=0.8 mol•L-1•s-1 | D. | v (D)=1 mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H3O+的电子式: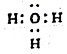 | |
| B. | 氨基的结构式:-NH2 | |
| C. | 乙烷的二氯代物有两种(不考虑立体异构) | |
| D. | NaHS显碱性的原因:HS-+H2O?S2-+H3O+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 体积相等时密度不相等 | B. | 原子数相等时具有的中子数不相等 | ||
| C. | 体积相等时具有的电子数相等 | D. | 质量相等时具有的质子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量氯气与乙烷在光照条件下反应(氯乙烷) | |
| B. | 乙烯与水加成(乙醇) | |
| C. | 乙烯与氯气加成(1,2-二氯乙烷) | |
| D. | 乙烯与氢气加成(乙烷) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com