
| 时间(s) C(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
| C(N2O4) | 0.20 | a | 0.10 | c | d | e |
| C(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
分析 (1)依据反应条件分析判断,结合化学平衡的三段式列式计算分析比较;
(2)化学平衡的三段式列式计算,结合化学反应速率概念计算0~20s内N2O4的平均反应速率;
(3)依据化学方程式和平衡常数概念写出平衡常数表达式,依据80°C平衡状态下结合三段式列式计算平衡浓度计算平衡常数.
解答 解:(1)将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,反应的化学方程式为:N2O4?2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据:反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅,说明反应逆向进行,逆向是放热反应,正向是吸热反应;依据化学平衡三段式列式计算分析判断,进行到40S和进行到60S时:
N2O4?2NO2
起始量(mol) 0.4 0
变化量(mol) 0.2 0.4
40S末(mol) 0.2 0.4
得到b=0.2mol/L;
进行到60S和进行到60S时:
N2O4?2NO2
起始量(mol) 0.4 0
变化量(mol) 0.22 0.44
60S末(mol) 0.18 0.44
c=0.18 mol/L
计算比较可知b>c;
故答案为:N2O4?2NO2;>;
(2)进行到20s;
N2O4?2NO2
起始量(mol) 0.4 0
变化量(mol) 0.12 0.24
20s末(mol) 0.28 0.24
0~20s内N2O4的平均反应速率=$\frac{\frac{0.12mol}{2L}}{20s}$=0.003mol/(L•s);
故答案为:0.003mol/(L•s);
(3)N2O4?2NO2,该反应的平衡常数为:K=$\frac{{c}^{2}(N{O}_{2})}{c({N}_{2}{O}_{4})}$;
80°C平衡状态和60s是相同平衡状态,平衡浓度c(NO2)=0.22mol/L,c(N2O4)=0.09mol/L;
平衡常数K=$\frac{{c}^{2}(N{O}_{2})}{c({N}_{2}{O}_{4})}$=$\frac{0.2{2}^{2}}{0.09}$=0.54mol/L;
故答案为:$\frac{{c}^{2}(N{O}_{2})}{c({N}_{2}{O}_{4})}$;0.54.
点评 本题考查了化学平衡的计算,题目难度中等,注意掌握化学平衡及其影响,明确三段式在化学平衡计算中的应用方法,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S) | |
| B. | Na2C2O4溶液:c(OH-)═c(H+)+c(HC2O4-)+2c(H2C2O4) | |
| C. | Na2CO3溶液:c(Na+)+c(H+)═2c(CO32-)+c(OH-) | |
| D. | CH3COONa和CaCl2溶液:c(Na+)+c(Ca2+)═c(CH3COO-)+c(OH-)+c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它们的表面都电镀上一层耐腐蚀的黄金 | |
| B. | 环境污染日趋严重,它们表面的铜绿被酸雨溶解洗去 | |
| C. | 铜的金属活动性比氢小,因此不易被氧化 | |
| D. | 它们是含一定比例金、银、锡、锌的铜合金 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大c(CH3COOH),b增大 | B. | 加水稀释,b减小 | ||
| C. | b的大小只与温度有关 | D. | 以上说法均不对 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
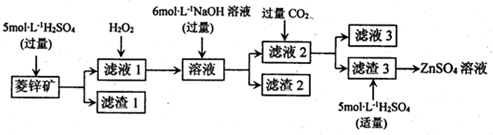
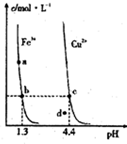 ②常温下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH.金属阳离子浓度的变化如图所示,下列判断正确的是BC.
②常温下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH.金属阳离子浓度的变化如图所示,下列判断正确的是BC.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 实验目的 | |
| A | 向苯和苯酚混合溶液中滴加过量浓溴水 | 除去混合溶液中的苯酚 |
| B | 向待测液中加入饱和碳酸钠溶液 | 鉴别乙酸、乙酸乙酯、乙醇 |
| C | 向3mL5%CuSO4溶液中滴加3-4滴1%氢氧化钠溶液,再向其中加入0.5mL乙醛,加热 | 检验醛基 |
| D | 将溴乙烷与氢氧化钠溶液共热,冷却,继续滴加硝酸银溶液 | 检验溴乙烷中的溴元素 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com