
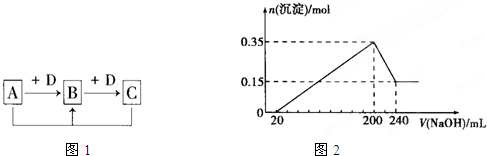
| 0.9mol |
| 0.2L-0.02L |


 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
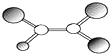 ��ͼ����ij���л�����ӵ����ģ��ͼ��ͼ�еġ���������������˫������ͬ��С�ġ��������ֲ�ͬ�Ķ�����Ԫ�ص�ԭ�ӣ��Ը��л������������ȷ���ǣ�������
��ͼ����ij���л�����ӵ����ģ��ͼ��ͼ�еġ���������������˫������ͬ��С�ġ��������ֲ�ͬ�Ķ�����Ԫ�ص�ԭ�ӣ��Ը��л������������ȷ���ǣ�������| A�����л�����ܵķ���ʽΪC2HCl3 |
| B�����л���ķ�����һ����C�TC�� |
| C�����л�������е�����ԭ����ͬһƽ���� |
| D�����л������γɵĻ�ѧ�����Ǽ��Լ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
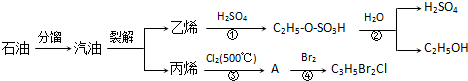
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ɫʯ����Һ | B������������Һ |
| C��ϡ���� | D��ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���������ƣ���ɫ���� |
| B��ɽ���ᣨ�������� |
| C�������ᣨ�������� |
| D��ά���أ�Ӫ��ǿ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ȼú���� |
| B����������ϵͳ��װ����װ�� |
| C�����̴��е��̽��о������ |
| D��ֲ�����֣�������Ⱦ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A����װ��֮��ȱ�ٸ���װ�� |
| B����װ���е�CuO��ĩ���ܲ����� |
| C��CuOû��ȫ������ԭ |
| D����װ�ú�ȱ�ٸ���װ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ٺ͢ڲ�����������Ӹ����Ȳ���� |
| B���ٺ͢����ɵ����ʵ����IJ��ת�Ƶ�������ͬ |
| C��������Na������O2��Ӧ����Na2O�����¶���������Na2O�������ӿ� |
| D��25�桢101 kPa�£�Na2O2��s��+2Na��s���T2Na2O��s������H=-317 kJ/mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com