
| A. | 显蓝色的淀粉溶液中通入足量的SO2后变成无色溶液:I2+SO2+2H2O═2I-+SO42-+4H+ | |
| B. | 向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| C. | 碳酸氢钙溶液中滴加氢氧化钠溶液至Ca2+恰好完全沉淀:Ca2++HCO3-+OHˉ═CaCO3↓+H2O | |
| D. | 盛放烧碱溶液的试剂瓶不能用玻璃塞:SiO2+2OH-═SiO32-+H2O |
分析 A.碘单质能够将二氧化硫氧化成硫酸;
B.硫酸根离子完全沉淀时,铝离子与氢氧根离子的物质的量之比为1:4,反应产物为偏铝酸根离子;
C.钙离子恰好沉淀时,二者物质的量为1:1;
D.二氧化硅与氢氧化钠溶液反应生成硅酸钠和水.
解答 解:A.显蓝色的淀粉溶液中通入足量的SO2后发生反应:I2+SO2+2H2O═2I-+SO42-+4H+,导致蓝色溶液变成无色,故A正确;
B.向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀,铝离子完全转化成偏铝酸根离子,Al3++2SO42-+4OH-+2Ba2+═2BaSO4↓+AlO2-+2H2O,故B错误;
C.碳酸氢钙溶液中滴加氢氧化钠溶液至Ca2+恰好完全沉淀,反应的离子方程式为:Ca2++HCO3-+OHˉ═CaCO3↓+H2O,故C正确;
D.由于发生反应SiO2+2OH-═SiO32-+H2O,则盛放烧碱溶液的试剂瓶不能用玻璃塞,故D正确;
故选B.
点评 本题考查了离子方程式的书写判断,为高考的高频题,题目难度不大,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:选择题
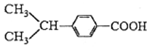 与
与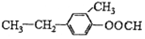
| A. | ①②③④ | B. | ①②③ | C. | ①②④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向盐酸中滴入少量偏铝酸钠溶液:AlO2-+H++H2O=Al(OH)3↓ | |
| B. | 向NaClO溶液中通入少量SO2:2ClO-+SO2+H2O═2HClO+SO32- | |
| C. | Cl2通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 用过量氨水吸收工业尾气中的SO2:2NH3•H2O+SO2═2NH4++SO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 体积为1ml、浓度均为0.10mol/L的XOH和X2CO3溶液,分别加水稀释至体积V,pH随lgV的变化情况如图所示,下列叙述中正确的是( )
体积为1ml、浓度均为0.10mol/L的XOH和X2CO3溶液,分别加水稀释至体积V,pH随lgV的变化情况如图所示,下列叙述中正确的是( )| A. | XOH是弱碱 | |
| B. | pH=10的两种溶液中的c(X+ ):XOH大于X2CO3 | |
| C. | 已知H2CO3的电离平衡常数Ka1远远大于Ka2,则Ka2约为1.0×10-10 | |
| D. | 当lgV=2时,若X2CO3溶液升高温度,溶液碱性增强,则c(HCO3-)/c(CO32- )减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 L 0.1 mol/L的NaHSO3溶液中含HSO3-的数目为0.1NA | |
| B. | 已知2SO2(g)+O2(g)?2SO3(g)△H=-196.6 kJ/mol,则将1 mol SO2与足量O2混合后充分反应放出的热量为98.3 kJ | |
| C. | 惰性电极电解硫酸铜的溶液,当阳极生成6.4 g铜时,阴极产生的气体在标准状况下为1.12 L | |
| D. | 金属发生吸氧腐蚀时,消耗1 mol O2,转移电子数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
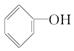 B.
B.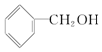 C.CH3 CH2-O-CH2CH3 D.CH3 OH E.CH3-O-CH3 F.HO-CH2CH2-OH
C.CH3 CH2-O-CH2CH3 D.CH3 OH E.CH3-O-CH3 F.HO-CH2CH2-OH查看答案和解析>>
科目:高中化学 来源: 题型:选择题
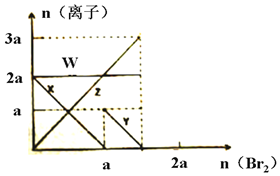 已知氧化性:Br2>Fe3+>I2,向amolFeI2和amolBaCl2的混合溶液中缓慢通入bmolBr2,并不断搅拌,溶液中离子的物质的量随Br2加入的变化如图所示(不考虑盐类水解、水的电离及溶液体积变化).则下列说法不正确的是( )
已知氧化性:Br2>Fe3+>I2,向amolFeI2和amolBaCl2的混合溶液中缓慢通入bmolBr2,并不断搅拌,溶液中离子的物质的量随Br2加入的变化如图所示(不考虑盐类水解、水的电离及溶液体积变化).则下列说法不正确的是( )| A. | 离子的还原性I->Fe2+>Br- | |
| B. | 四条线与溶液中离子的对应关系是:X-Fe2+、Y-I-、Z-Br-、W-Cl- | |
| C. | 当4a=3b时,反应后的离子浓度比:c(Fe2+):c(Fe3+)c:(Br-)=1:2:8 | |
| D. | 当3a≤2b时,发生的离子方程式:2Fe2++4I-+3Br2═2Fe3++2I2+6Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ②④ | C. | ②③④ | D. | ①②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com