
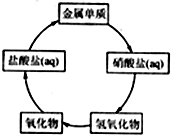
 在一定条件下,五种含有同种金属元素的单质或其化合物,能按有图箭头方向实现一步转化(不含电解),该金属元素可能是 ( )
在一定条件下,五种含有同种金属元素的单质或其化合物,能按有图箭头方向实现一步转化(不含电解),该金属元素可能是 ( )| A. | ①② | B. | ②④ | C. | ①③ | D. | ③④ |
分析 根据图示可知,金属的盐酸盐能够一步转化成金属单质(不含电解),该反应为置换反应,较活泼金属无法实现,如Al、Na,而Fe、Cu两种金属可以按照图示实现一步转化,据此进行解答.
解答 解:①Fe能够与硝酸反应生成硝酸铁,硝酸铁与氢氧化钠反应生成氢氧化铁沉淀,氢氧化铁加热生成氧化铁,氧化铁与元素反应生成氯化铁,氯化铁与锌反应生成铁,铁及其化合物均能够按照图示箭头通过一步反应完成,故①正确;
②Cu与硝酸反应生成硝酸铜,硝酸铜与氢氧化钠溶液反应生成氢氧化铜沉淀,氢氧化铜加热分解生成氧化铜,氧化铜与盐酸反应生成氯化铜,氯化铜与铁反应生成铜,所以Cu满足题中转化关系,故②正确;
③Al的硝酸盐为硝酸铝,硝酸铝(除电解外)无法一步反应转化成Al,故③错误;
④硝酸钠无法一步转化成氢氧化钠,氢氧化钠也无法一步生成氧化钠,氯化钠也无法一步生成金属钠(除电解方法),故④错误;
故选A.
点评 本题考查了常见金属元素及其化合物性质,题目难度中等,明确常见元素及其化合物性质为解答关键,试题侧重基础知识的考查,培养了学生的分析能力及灵活应用能力.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:选择题
 海洋中的珊瑚虫经如下反应形成石灰石外壳,进而形成珊瑚:Ca2++2HCO3-?CaCO3+H2O+CO2.与珊瑚虫共生的藻类会消耗海洋中的CO2.气候变暖、温室效应的加剧干扰了珊瑚虫的生长,甚至致其死亡.下列说法不合理的是( )
海洋中的珊瑚虫经如下反应形成石灰石外壳,进而形成珊瑚:Ca2++2HCO3-?CaCO3+H2O+CO2.与珊瑚虫共生的藻类会消耗海洋中的CO2.气候变暖、温室效应的加剧干扰了珊瑚虫的生长,甚至致其死亡.下列说法不合理的是( )| A. | 共生藻类消耗CO2,有利于珊瑚的形成 | |
| B. | 海洋中CO2浓度升高,抑制了珊瑚的形成 | |
| C. | 温度升高会增大CO2在海水中的溶解度,抑制了珊瑚的形成 | |
| D. | 将CO2转化为甲醇等化工原料,有助于缓解温室效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇用作医用消毒剂时,无水乙醇消毒效果最好 | |
| B. | 高锰酸钾溶液可以杀死埃博拉病毒,其消毒原理与漂白粉消毒饮用水的原理不同 | |
| C. | 公益调查《柴静雾霾调查:穹顶之下》发布,其中雾霾中的PM2.5属于胶体 | |
| D. | 天津港爆炸案中对剧毒的氰化钠(NaCN) 喷洒双氧水处理,利用了双氧水的氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉中加入浓盐酸:ClO-+Cl-+2H+═Cl2↑+H2O | |
| B. | 氯化铁溶液洗涤银镜:Fe3++Ag═Fe2++Ag+ | |
| C. | 0.1 mol•L-1NH4HSO4溶液和0.1 mol•L-1NaOH等体积混合:NH4++H++2OH-═NH3•H2O+H2O | |
| D. | 0.1 mol•L-1的NaAlO2溶液和0.15 mol•L-1的H2SO4溶液等体积混合:AlO2-+4H+═Al3++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
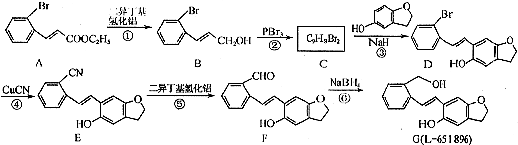
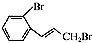 .
.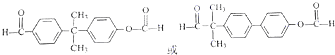 (只写一种).
(只写一种).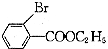 为原料制备二氢异苯并呋喃(结构简式如图
为原料制备二氢异苯并呋喃(结构简式如图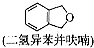 )的合成路线流程图(无机试剂可任选).
)的合成路线流程图(无机试剂可任选).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.2mol/L | B. | 1.4mol/L | C. | 1.7mol/L | D. | 1.9mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化碳的电子式: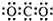 | |
| B. | 氯离子的结构示意图: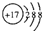 | |
| C. | NaH与重水反应的化学方程式:NaH+D2=NaOH+D2 | |
| D. | 质量数为18的氧原子:${\;}_{6}^{18}$O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
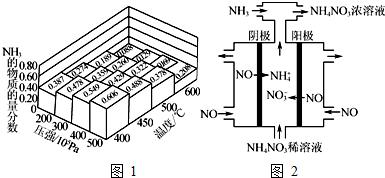
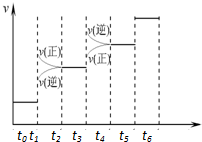 已知N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ•mol-1.请回答:(1)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如右图所示.图中tl时引起平衡移动的条件可能是增大压强.其中表示平衡混合物中NH3的含量最高的一段时是t2-t3.
已知N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ•mol-1.请回答:(1)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如右图所示.图中tl时引起平衡移动的条件可能是增大压强.其中表示平衡混合物中NH3的含量最高的一段时是t2-t3.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com