
| 成分 | 质量(g) | 摩尔质量(g•mol-1) |
| 蔗糖 | 25.00 | 342 |
| 硫酸钾 | 0.87 | 174 |
| 阿司匹林 | 0.17 | 180 |
| 高锰酸钾 | 0.316 | 158 |
| 硝酸银 | 0.075 | 170 |
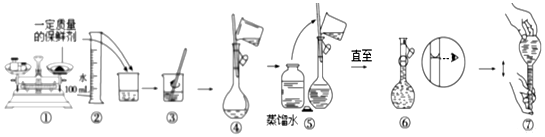
分析 (1)在水溶液或者熔融状态下能够导电的化合物为电解质,在水溶液荷熔融状态下都不能够导电的化合物为非电解质;
(2)依据配制一定物质的量浓度溶液的一般步骤选择需要仪器;
(3)根据托盘天平的使用方法判断;依据定容的正确操作解答;
(4)分析操作对溶质的物质的量或对溶液的体积的影响,根据c=$\frac{n}{V}$分析判断.
解答 解:(1)A.蔗糖 在水溶液荷熔融状态下都不能够导电的化合物为非电解质,故A选;
B.硫酸钾在水溶液或者熔融状态下能够导电的化合物为电解质,故B不选;
C.高锰酸钾在水溶液或者熔融状态下能够导电的化合物为电解质,故C不选;
D.硝酸银在水溶液或者熔融状态下能够导电的化合物为电解质,故D不选;
故选:A;
(2)配制一定物质的量浓度溶液的一般步骤:计算、称量、溶解、移液、洗涤、定容、摇匀等,用到的仪器:托盘天平、烧杯、玻璃棒、容量瓶、胶头滴管,配制500mL,应选择500mL规格容量瓶,所以还缺少的仪器:500mL容量瓶、胶头滴管;
故答案为:500mL容量瓶;胶头滴管;
(3)错误的操作步骤有:①没有按照左物右码的规定称量药品;⑤定容时,加蒸馏水到离刻度线1-2cm,改用胶头滴管逐滴滴加,
故答案为:①⑤;
(4)A.溶解固体时,未冷却就直接转移,导致溶液体积偏小,溶液浓度偏高,故A选;
B.转移溶液后未洗涤烧杯和玻璃棒就直接定容,导致溶质部分损耗,溶质的物质的量偏小,溶液浓度偏低,故B不选;
C.在容量瓶中定容时俯视刻度线,导致溶液体积偏小,溶液浓度偏高,故C选;
D.定容后把容量瓶倒转摇匀,发现液面低于刻度,再补充几滴水至刻度,导致溶液体积偏大,溶液浓度偏低,故D不选;
故选:AC.
点评 本题主要考查了一定物质的量浓度的配制步骤、仪器和误差分析,明确配制原理及操作步骤是解题关键,注意误差分析方法.


科目:高中化学 来源:2016-2017学年甘肃省高二上10月月考化学试卷(解析版) 题型:选择题
有一支50mL酸式滴定管其中盛有溶液,液面恰好在10mL刻度处,现把管内溶液全部流下排出,用量筒承接,该溶液的体积应为
A.10mL B.40mL C.大于40mL D.小于40mL
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相等 | B. | 后者是前者的11倍 | ||
| C. | 后者是前者的108 | D. | 前者是后者的108 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用催化剂,可加快反应速率,目的是提高生产效率 | |
| B. | 使用冰箱保存食物,是利用了化学反应速率理论 | |
| C. | 化学反应速率理论是研究怎样提高原料转化率 | |
| D. | 化学平衡理论是研究怎样使用有限原料多出产品 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
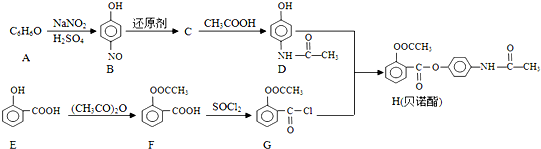
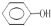 ;E中含氧官能团的名称为羟基、羧基.
;E中含氧官能团的名称为羟基、羧基.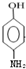 .
.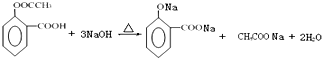 .
.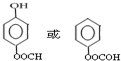 .
.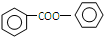 的合成路线流程图(无机试剂可任选):
的合成路线流程图(无机试剂可任选):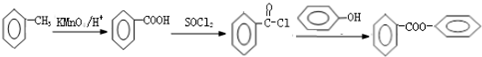 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
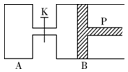 图中,P为一可自由滑动的活塞,关闭K,分别向容器A、B中各充入1mol X、1mol Y,起始时,VA=a L,VB=0.8a L(连通管的体积忽略不计),在相同温度和有催化剂存在的条件下,两容器中各自发生下述反应:3X(g)+3Y(g)?2Z(g)+2W(g),达平衡时,VB=0.6a L.回答下列问题:
图中,P为一可自由滑动的活塞,关闭K,分别向容器A、B中各充入1mol X、1mol Y,起始时,VA=a L,VB=0.8a L(连通管的体积忽略不计),在相同温度和有催化剂存在的条件下,两容器中各自发生下述反应:3X(g)+3Y(g)?2Z(g)+2W(g),达平衡时,VB=0.6a L.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
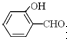 形成分子内氢键,而
形成分子内氢键,而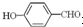 形成分子间氢键,分子间氢键使分子间作用力增大.
形成分子间氢键,分子间氢键使分子间作用力增大.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 已知Zn+CuSO4═Cu+ZnSO4,设计原电池:构造如图1所示,试问ZnSO4溶液放在甲(填“甲”或“乙”)烧杯,盐桥中的离子向两端烧杯移动,构成闭合回路,K+移向乙(填“甲”或“乙”)烧杯.
已知Zn+CuSO4═Cu+ZnSO4,设计原电池:构造如图1所示,试问ZnSO4溶液放在甲(填“甲”或“乙”)烧杯,盐桥中的离子向两端烧杯移动,构成闭合回路,K+移向乙(填“甲”或“乙”)烧杯.查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上10月月考化学试卷(解析版) 题型:选择题
在水中加入下列物质 ,可使水的电离平衡正向移动的是( )
,可使水的电离平衡正向移动的是( )
A.NaOH B.NH4Cl C.NaCl D.H2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com