
【题目】下列说法正确的是( )
A.NaHCO3溶液加水稀释,c(Na+)/c(HCO3-)的比值保持增大
B.浓度均为0.1 mol·L-1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO32-)+c(HCO3-)]
C.在高锰酸钾溶液中,H+、K+、SO42-、葡萄糖分子可以大量共存
D.已知:Ksp(AgCl)=1.8×10-10, Ksp(Ag2Cr2O4)=2.0×10-12,则Ag2CrO4的溶解度小于AgCl
【答案】A
【解析】
A. ![]() =
=![]() ,NaHCO3溶液加水稀释时,n(Na+)保持不变,n(HCO3-)减小,所以c(Na+)/c(HCO3-)的比值保持增大,A选项正确;
,NaHCO3溶液加水稀释时,n(Na+)保持不变,n(HCO3-)减小,所以c(Na+)/c(HCO3-)的比值保持增大,A选项正确;
B. 根据物料守恒,浓度均为0.1 mol·L-1的Na2CO3、NaHCO3混合溶液:3c(Na+)=2[c(CO32-)+c(HCO3-)],B选项错误;
C. 高锰酸钾会氧化葡萄糖,C选项错误;
D. 假设Ag2CrO4饱和溶液中Ag+的浓度为x,则CrO42-的浓度为0.5x,由溶度积常数的表达式可知Ksp(Ag2CrO4)=x2×0.5x=0.5x3=2.0×10-12,x3=4.0×10-12,即x═![]() ,因为AgCl饱和溶液中Ag+的浓度为
,因为AgCl饱和溶液中Ag+的浓度为![]() ,所以的溶解度大于AgCl,D选项错误;
,所以的溶解度大于AgCl,D选项错误;
答案选A。


科目:高中化学 来源: 题型:
【题目】NaBH4燃料电池具有理论电压高、能量密度大等优点。以该燃料电池为电源电解精炼铜的装置如图所示。下列说法不正确的是

A. 离子交换膜应为阳离子交换膜,Na+由左极室向右极室迁移
B. 该燃料电池的负极反应式为BH4-+8OH--8e-=BO2-+6H2O
C. 电解池中的电解质溶液可以选择CuSO4溶液
D. 每消耗2.24LO2(标准状况)时,A电极的质量减轻12.8g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某温度时,水的离子积Kw=1×10-13,则该温度_________25℃(填“>”、“<”或“=”)。在此温度下,某溶液中由水电离出来的H+浓度为1×10-10molL-1,则该溶液的pH可能为________;
(2)若温度为25℃时,体积为Va、pH=a的H2SO4与体积为Vb、pH=b的NaOH混合,恰好中和,此溶液中各种离子的浓度由大到小的排列顺序是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.2.0gH218O与2H2O的混合物中所含中子数约为6.02×1023
B.2Mg(s)+CO2(g)=C(s)+2MgO(s)在一定条件下能自发进行,说明该反应的△H<0
C.向硫酸钡悬浊液中加入足量饱和Na2CO3溶液,振荡、过滤、洗涤,向沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3)
D.向浑浊的苯酚试液中加饱和Na2CO3溶液,试液变澄清,说明苯酚的酸性强于碳酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨反应N2 ( g ) +3H2 ( g ) = 2NH3 ( g ) ,反应过程的能量变化如图所示。已知N2 ( g ) 与 H2( g )反应生成 17 gNH3(g),放出46. 1kJ的热量。请回答下列问题:

(1)该反应通常用铁作催化剂,加催化剂会使图中E_______________(填“变大”或“变小”) ,E 的大小对该反应的反应热有无影响?___________,理由是__________。
(2)图中△H=________kJ·mol -1。
(3)起始充入2mol·L-1N2和5.5mol·L-1H2,经过50min,NH3的浓度为1mol·L-1,则v(N2)=______mol·L-1·min-1,c(H2)=_____mol·L-1
(4)已知NH3(g)=NH3(l) △H=-QkJ·mol-1,则N2 ( g ) +3H2 ( g ) = 2NH3 ( l )的△H=_______kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四个图像所反映的内容与相应反应符合的是(a、b、c、d均大于0)( )
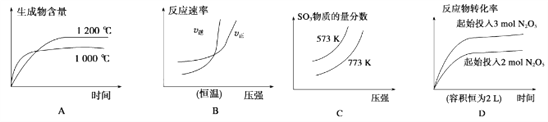
A. 4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)ΔH=-akJ·mol-1
4NO(g)+6H2O(g)ΔH=-akJ·mol-1
B. N2(g)+3H2(g)![]() 2NH3(g)ΔH=-bkJ·mol-1
2NH3(g)ΔH=-bkJ·mol-1
C. 2SO3(g)![]() 2SO2(g)+O2(g)ΔH=+ckJ·mol-1
2SO2(g)+O2(g)ΔH=+ckJ·mol-1
D. 2N2O5(g)![]() 4NO2(g)+O2(g)ΔH=+dkJ·mol-1
4NO2(g)+O2(g)ΔH=+dkJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】还原沉淀法是处理含铬(含Cr2O72-和CrO42-)工业废水的常用方法,过程如下:![]()
已知转化过程中的反应为2CrO42﹣(aq)+2H+(aq)![]() Cr2O72﹣(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO42-有10/11转化为Cr2O72-,下列说法不正确的是( )
Cr2O72﹣(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO42-有10/11转化为Cr2O72-,下列说法不正确的是( )
A. 溶液颜色保持不变,说明上述可逆反应达到平衡状态
B. 若用绿矾(FeSO4·7H2O)作还原剂,处理1L废水,至少需要917.4 g
C. 常温下转化反应的平衡常数K=l×1014.则转化后所得溶液的pH=6
D. 常温下Ksp[Cr(OH)3]=1×10-32,要使处理后废水中的c(Cr3+)降至1×10-5mol/L,应调溶液的pH=5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+ B(g)![]() C(g) +2D(g)的能量变化如图所示,回答下列问题。
C(g) +2D(g)的能量变化如图所示,回答下列问题。

(1)该反应是_______________反应(填“吸热”“放热”)。
(2)当反应达到平衡时,升高温度,A的转化率_______(填“增大”“减小”“不变”下同),原因是__________________;
(3)向体系中加入催化剂,△H_____________;
(4)向体系中加入催化剂,反应速率增大,E1和E2的变化是E1______E2_____ ;
(5)将1molA和2molB加入2L容器中,5min后达到平衡,此时A的转化率为50%,则5min内用D表示化学反应速率为___________平衡常数K=________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】毒奶粉事件震惊全国,这主要是奶粉中含有有毒的三聚氰胺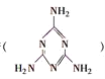 。下列关于三聚氰胺分子的说法正确的是( )
。下列关于三聚氰胺分子的说法正确的是( )
A.所有碳原子采用sp3杂化,所有氮原子采用sp3杂化
B.一个分子中共含有15个σ键
C.属于极性分子,故极易溶于水
D.分子内既有极性键又有非极性键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com