
| A. | O2通入正极区 | |
| B. | 总反应为:2H2+O2═2H2O | |
| C. | 正极发生氧化反应 | |
| D. | 负极区电极反应为 2H2+4OH--4e-═4H2O |
分析 根据燃料电池的工作原理和规律:氢氧燃料电池是将化学能转变为电能的装置,工作时,通入燃料氢气的一极为电池的负极,发生氧化反应,通入氧气的一极为电池的正极,发生还原反应,电池总反应与氢气在氧气中燃烧的化学方程式一致,产物为水.
解答 解:A、在燃料电池中,通入氧气的一极为电池的正极,故A正确;
B、电池总反应与氢气在氧气中燃烧的化学方程式一致即2H2+O2═2H2O,故B正确;
C、通入氧气的一极为电池的正极,发生还原反应,故C错误;
D、通入燃料氢气的一极为电池的负极,发生氧化反应,因为KOH溶液作电解液,所以电极反应为2H2+4OH--4e-═4H2O,故D正确.
故选C.
点评 本题考查学生燃料电池的工作原理以及电极反应方程式的书写知识,属于基本知识的考查,难度不大,关键在于区分正极反应和负极,以及正负极发生的反应.


科目:高中化学 来源:2016-2017学年云南省高一9月月考化学卷(解析版) 题型:选择题
在一定条件下,RO3n-和氟气可发生如下反应:RO3n- + F2 + 2OH- == RO4- + 2F- + H2O,从而可知在RO3n-中,元素R的化合价是
A.+4 B.+5 C.+6 D.+7

查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
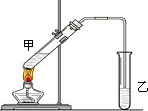 俗话说,“陈酒老醋特别香”,其原因是酒在储存过程中生成了有香味的乙酸乙酯,在实验室里我们也可以用如图所示的装置来模拟该过程.请回答下列问题:
俗话说,“陈酒老醋特别香”,其原因是酒在储存过程中生成了有香味的乙酸乙酯,在实验室里我们也可以用如图所示的装置来模拟该过程.请回答下列问题: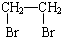 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
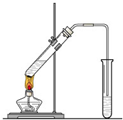 在实验室我们也可以用右图所示的装置制取乙酸乙酯.
在实验室我们也可以用右图所示的装置制取乙酸乙酯.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
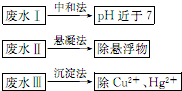 水处理技术在生产、生活中应用广泛,对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施.
水处理技术在生产、生活中应用广泛,对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
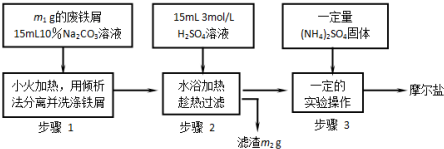
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
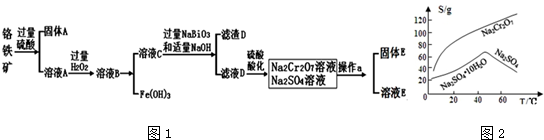
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com