
| A�� | 0.1 mol•L-1 Na2CO3��Һ�У�c��HCO3-��=2c��H2CO3��+c��H+��-c��OH-�� | |
| B�� | ���ʵ���Ũ����ȵ�Na2SO3��NaHSO3��Һ�У�3c��Na+��=2[c��HSO3-��+c��H2SO3��+c��SO32-��] | |
| C�� | ͬŨ�ȵ�������Һ�У���NH4HSO4 ��NH4Cl ��NH3•H2O��c��NH4+���ɴ�С��˳���ǣ��ڣ��٣��� | |
| D�� | �����£�Ũ�Ⱦ�Ϊ0.1mol/L NaA��HA��Һ��pH=8��c��HA����c��Na+����c��A-����c��OH-����c��H+�� |
���� A����Һ�д��ڵ���غ㡢�����غ㣬��������ж�ѡ�
B����Һ�д��������غ㣬2n��Na��=3n��S����
C����NH4HSO4 ��Һ������������笠���ˮ�⣬��NH4Cl��Һ�������Ӷ�笠�����Ũ����Ӱ�죬��NH3•H2O��������������룻
D�������£�Ũ�Ⱦ�Ϊ0.1mol/L NaA��HA��Һ��pH=8����Һ�Լ��ԣ�˵��A-����ˮ��̶ȴ���HA�ĵ���̶ȣ��ݴ˷�������Ũ�ȴ�С��
��� �⣺A����Һ�д��ڵ���غ㣺c��H+��+c��Na+��=c��OH-��+c��HCO3-��+2c��CO32-���������غ�Ϊ��2c��CO32-��+2c��HCO3-��+2c��H2CO3��=c��Na+��������õ�c��HCO3-��+2c��H2CO3��+c��H+��=c��OH-������A����
B�����ʵ���Ũ����ȵ�Na2SO3��NaHSO3��Һ�д��������غ㣬2c��Na+��=3[c��HSO3-��+c��H2SO3��+c��SO32-��]����B����
C����NH4HSO4 ��Һ������������笠���ˮ�⣬��NH4Cl��Һ�������Ӷ�笠�����Ũ����Ӱ�죬��NH3•H2O��������������룬ͬŨ�ȵ���Һ�У���NH4HSO4 ��NH4Cl ��NH3•H2O��c��NH4+���ɴ�С��˳���ǣ��٣��ڣ��ۣ���C����
D�������£�Ũ�Ⱦ�Ϊ0.1mol/L NaA��HA��Һ��pH=8����Һ�Լ��ԣ�˵��A-����ˮ��̶ȴ���HA�ĵ���̶ȣ�c��HA����c��Na+����c��A-����c��OH-����c��H+������D��ȷ��
��ѡD��
���� ���⿼��������ˮ��ԭ�����������Һ�е���غ㡢�����غ㡢�����غ����д�ͼ���Ӧ�ã�ע������ˮ���ʱ��Һ����Ե��жϣ���Ŀ�Ѷ��еȣ�


 ����ѧ��Ӧ�����ϵ�д�
����ѧ��Ӧ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���н�������A��B��C������ס��ҡ���������D��E��F��G�����ɫ����H����֪����ɫ������ΪCl2������֮���ܷ������·�Ӧ��ͼ����Щ��Ӧ�IJ���ͷ�Ӧ������û��ȫ��������������������Ϣ�ش��������⣺
���н�������A��B��C������ס��ҡ���������D��E��F��G�����ɫ����H����֪����ɫ������ΪCl2������֮���ܷ������·�Ӧ��ͼ����Щ��Ӧ�IJ���ͷ�Ӧ������û��ȫ��������������������Ϣ�ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ������ | Fe3+ | Fe2+ | Cu2+ |
| ��ʼ����ʱ��pH | 1.9 | 7.0 | 4.7 |
| ������ȫʱ��pH | 3.2 | 9.0 | 6.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
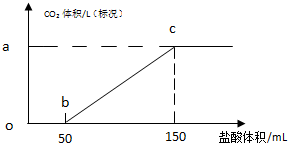
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
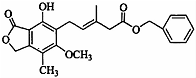
| A�� | ���������е�ԭ�ӹ�ƽ�� | |
| B�� | �ȿ�����FeCl3��Һ������ɫ��Ӧ���ֿ�����NaHCO3��Һ��Ӧ�ų�CO2���� | |
| C�� | 1 mol�û�������������9mol H2�����ӳɷ�Ӧ | |
| D�� | �������ܷ���ȡ����Ӧ��������Ӧ���ӳɷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2�� | B�� | 3�� | C�� | 4�� | D�� | 5�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ѧʵ����ͻ�����Ч�ؼ�����Ⱦ��ʵ�ֻ�ѧʵ����ɫ����Ҫ��ijѧ�������в�����һ��ʵ�飺��һ���³İ�ֽ�IJ���Ƭ�IJ�ͬλ�÷ֱ�μ�Ũ��Ϊ0.1mol/L��KBr��KI���� ������Һ����NaOH������̪����FeCl2����KSCN����Һ��1�Σ�ÿ��Һ�α˴˷ֿ���Χ�ɰ뾶С�ڱ������Բ�Σ�����ͼ��ʾ������Բ�Ĵ�����2��֥������С��KMnO4���壬��KMnO4����μ�һ��Ũ���ᣬ��������������Ǻã�����֪��2KMnO4+16HCl��Ũ���T2KCl+2MnCl2+5Cl2��+8H2O��
��ѧʵ����ͻ�����Ч�ؼ�����Ⱦ��ʵ�ֻ�ѧʵ����ɫ����Ҫ��ijѧ�������в�����һ��ʵ�飺��һ���³İ�ֽ�IJ���Ƭ�IJ�ͬλ�÷ֱ�μ�Ũ��Ϊ0.1mol/L��KBr��KI���� ������Һ����NaOH������̪����FeCl2����KSCN����Һ��1�Σ�ÿ��Һ�α˴˷ֿ���Χ�ɰ뾶С�ڱ������Բ�Σ�����ͼ��ʾ������Բ�Ĵ�����2��֥������С��KMnO4���壬��KMnO4����μ�һ��Ũ���ᣬ��������������Ǻã�����֪��2KMnO4+16HCl��Ũ���T2KCl+2MnCl2+5Cl2��+8H2O���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com