
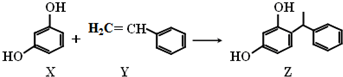
| A. | X、Y和Z均能与溴水发生反应,其中X、Z发生取代反应,Y发生加成反应 | |
| B. | X和Z均能NaOH溶液反应,也能与NaHCO3溶液反应放出CO2 | |
| C. | Y既能与H2发生加成反应,也能使酸性高锰酸钾溶液褪色 | |
| D. | Y可作加聚反应单体,X可作缩聚反应单体 |
分析 A.含有酚羟基,可与溴水发生取代反应,含有碳碳双键,可发生加成反应;
B.苯酚的酸性比碳酸弱;
C.Y含有碳碳双键,可发生加成、氧化反应;
D.Y含有碳碳双键,可发生加聚反应,X含有酚羟基,可与醛发生缩聚反应.
解答 解:A.X、Z含有酚羟基,可与溴水发生取代反应,Y含有碳碳双键,可发生加成反应,故A正确;
B.苯酚的酸性比碳酸弱,X和Z与碳酸氢钠不反应,故B错误;
C.Y含有碳碳双键,可与氢气发生加成、与高锰酸钾发生氧化反应,故C正确;
D.Y含有碳碳双键,可发生加聚反应,X含有酚羟基,可与醛发生缩聚反应,故D正确.
故选B.
点评 本题考查有机物的结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查酚、烯烃的性质,难度不大.


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .写出反应⑥的化学方程式:CH2BrCH2CH2Br+2NaOH$→_{△}^{水}$HOCH2CH2CH2OH+2NaBr.
.写出反应⑥的化学方程式:CH2BrCH2CH2Br+2NaOH$→_{△}^{水}$HOCH2CH2CH2OH+2NaBr. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
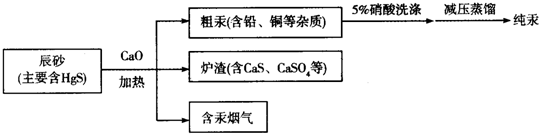
| A. | 流程中加入氧化钙的目的是减少SO2的排放 | |
| B. | “辰砂”加热时发生反应:HgS+O2$\frac{\underline{\;\;△\;\;}}{\;}$Hg+SO2,该方法属于热分解法 | |
| C. | 洗涤粗汞时可用5%的盐酸代替5%的硝酸 | |
| D. | 含汞烟气中汞的含量很低,可以直接排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
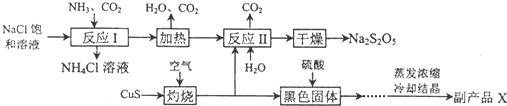
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锂盐 | B. | 钠盐 | C. | 钙盐 | D. | 铜盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
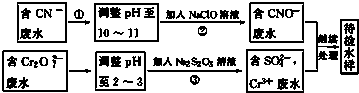
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com