
| A、升高温度 |
| B、加入少量的CuSO4溶液 |
| C、改用纯度高的锌粒 |
| D、改用小颗粒的锌粒 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该反应中C12是氧化剂 |
| B、若管道漏气遇氨会产生白烟 |
| C、该反应生成1 mol N2,有6 mol电子发生转移 |
| D、该反应中氨气发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸钾、碳酸钙、碳酸氢钙都属于可溶性的碳酸盐 |
| B、二氧化硫、五氧化二磷、乙醇都属于氧化物 |
| C、氢氧化钡、氢氧化钾、纯碱都属于碱 |
| D、盐酸、硝酸、乙酸都属于一元酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
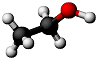
| A、可以与醋酸发生中和反应 |
| B、能与钠发生取代反应 |
| C、能使紫色石蕊试液变红色 |
| D、能发生催化氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 用导线把锌片与铜片连接好,然后平行插入稀硫酸中(如图所示),下列说法正确的是( )
用导线把锌片与铜片连接好,然后平行插入稀硫酸中(如图所示),下列说法正确的是( )| A、铜为负极 |
| B、铜片上无气泡产生 |
| C、锌片逐渐溶解 |
| D、锌片上有气泡产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、其原子的电子层比Br多一层 |
| B、其原子半径比Br的小 |
| C、其氢化物的稳定性比HBr强 |
| D、其单质的氧化性比Br2强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
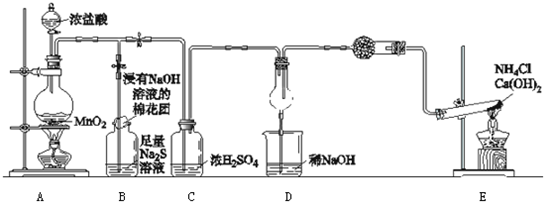
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com