
| A. | 化学反应中的能量变化都表现为热量的变化 | |
| B. | 需要加热才能发生的反应一定是吸热反应 | |
| C. | 放热反应在常温下一定很容易发生 | |
| D. | 反应是吸热还是放热必须看旧键断裂时吸收的能量和新键形成时释放的能量的大小 |
科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | ③⑤⑥ | C. | ④⑤⑥ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 比较镁、铝金属性:镁、铝(除氧化膜)分别放入4mol•L-1NaOH溶液中 | |
| B. | 比较氯、溴非金属性:氯气通入溴化钠溶液中 | |
| C. | 比较Cu、Fe2+的还原性:Cu加入FeCl3溶液中 | |
| D. | 比较高锰酸钾、氯气的氧化性:高锰酸钾中加入浓盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单地说,金属的冶炼就是把金属单质从其矿物中分离出来 | |
| B. | 金属冶炼过程中,被冶炼的金属只能被氧化 | |
| C. | 金属冶炼过程中,被冶炼的金属只能被还原 | |
| D. | 金属冶炼过程中,被冶炼的金属既可被氧化,也可被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
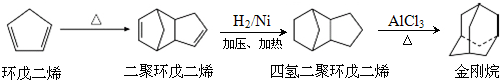
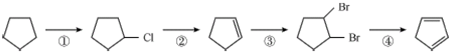
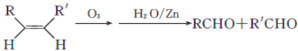

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO | B. | N2O3 | C. | N2O | D. | N2O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
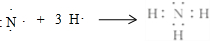
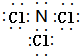
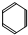 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
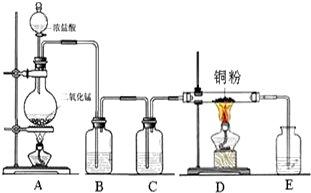 实验室里用如图所示装置制取纯净的无水CuCl2.试回答下列问题:
实验室里用如图所示装置制取纯净的无水CuCl2.试回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com