
| A、金刚石>晶体硅>二氧化硅>碳化硅 |
| B、MgO>O2>N2>H2O |
| C、CI4>CBr4>CCl4>CH4 |
| D、金刚石>生铁>纯铁>钠 |


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeS和CuS |
| B、FeS |
| C、CuS |
| D、Al2S3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| NaCl | MgCl2 | AlCl3 | SiCl4 | |
| 熔点/℃ | 801 | 714 | 190 | -70 |
| 沸点/℃ | 1 413 | 1 412 | 180 | 57.57 |
| A、①② | B、②③ | C、①②④ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4>SiH4>GeH4>SnH4 |
| B、KCl>NaCl>MgCl2>MgO |
| C、Rb>K>Na>Li |
| D、石墨>金刚石>SiO2>钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、烧碱的量不足 |
| B、乙醛的量不足 |
| C、硫酸铜的量不足 |
| D、加热时间短 |
查看答案和解析>>
科目:高中化学 来源: 题型:
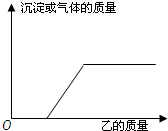 向下表中的甲物质中逐滴加入乙物质至过量,反应生成气体或沉淀的质量与加入的乙的质量关系符合如图所示曲线描述的是( )
向下表中的甲物质中逐滴加入乙物质至过量,反应生成气体或沉淀的质量与加入的乙的质量关系符合如图所示曲线描述的是( )| 序号 | 甲 | 乙 |
| A | 二氧化锰 | 过氧化氢溶液 |
| B | 氢氧化钠和碳酸钠混合溶液 | 稀盐酸 |
| C | 氯化钠和氢氧化钙的混合溶液 | 碳酸钠溶液 |
| D | 氯化铁和氯化铜溶液 | 氢氧化钠溶液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com