
 1915年诺贝尔物理学奖授予HenryBragg和LawrenceBragg,以表彰他们用X射线对晶体结构的分析所作的贡献.
1915年诺贝尔物理学奖授予HenryBragg和LawrenceBragg,以表彰他们用X射线对晶体结构的分析所作的贡献.| 晶体 | NaCl | KC1 | CaO |
| 晶格能/(kJ•mol-1) | 786 | 715 | 3401 |
分析 (1)影响晶体晶格能大小的因素有离子半径以及离子所带电荷的多少,晶格能越大熔点越高;基态Na原子核电电子排布式为1s22s22p63s1;
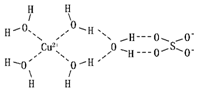
(2)①因为水分子间存在氢键,氢键会使水分子成为缔合水分子,使得体积变小,所以用蒸汽密度法测得的H2O的相对分子质量比理论计算出来的相对分质量较大;
②根据S原子的价电子对数进行判断;具有相同原子数和价电子数的微粒互称为等电子体;
③形成4个配位键,具有对称的空间构型,可能为平面正方形或正四面体,如为正四面体,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,只有一种结构;
④铜为29号元素,根据原子核外电子排布规律书写Cu2+外围电子排布式,根据均摊法计算出晶胞中铜原子数,Cu原子的半径为r pm,则晶胞的边长2$\sqrt{2}$r pm,晶胞的体积为(2$\sqrt{2}$r×10-10)3cm3,根据ρ=$\frac{m}{V}$计算密度.
解答 解:(1)离子半径Mg2+<Na+<O2-<Ca2+<Cl-;离子电荷数Na+=Cl-<O2-=Mg2+=Ca2+,离子晶体的离子半径越小,带电荷数越多,晶格能越大,则晶体的熔沸点越高,则有NaCl、KCl、MgO、CaO熔点由高到低的顺序是MgO>CaO>NaCl>KCl,根据基态Na原子的电子排布式可知Na原子核外有4个不同的能级;
故答案为:MgO>CaO>NaCl>KCl;4;
(2)①因为水分子间存在氢键,氢键会使水分子成为缔合水分子,使得体积变小,所以用蒸汽密度法测得的H2O的相对分子质量比理论计算出来的相对分质量较大,
故答案为:水分子间存在氢键,氢键会使水分子成为缔合水分子,所以计算出来的相对分子质量较大;
②SO42-中S的价电子对数=$\frac{6+2}{2}$=4,形成四条杂化轨道,S原子的杂化方式为sp3,具有相同原子数和价电子数的微粒互称为等电子体,所以与SO42-互为等电子体的微粒有ClO4-、PO43-等;
故答案为:sp3;ClO4-、PO43-等;
③形成4个配位键,具有对称的空间构型,可能为平面正方形或正四面体,如为正四面体,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,只有一种结构,所以应为平面正方形,
故答案为:平面正方形;
④铜为29号元素,其原子外围电子排布式为3d104s1,则Cu2+外围电子排布式为3d9;根据均摊法计算出晶胞中铜原子数为=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,Cu原子的半径为r pm,则晶胞的边长为2$\sqrt{2}$r pm,晶胞的体积为(2$\sqrt{2}$r×10-10)3cm3,所以铜的密度=$\frac{m}{V}$=$\frac{\frac{4×64}{{N}_{A}}}{(2\sqrt{2}r×1{0}^{-10})^{3}}$g/cm3=$\frac{4×64}{{N}_{A}(2\sqrt{2}r×1{0}^{-10})^{3}}$g/cm3,
故答案为:3d9;$\frac{4×64}{{N}_{A}(2\sqrt{2}r×1{0}^{-10})^{3}}$.
点评 本题考查的内容较杂,涉及到离子晶体的晶格能、金属晶体结构、配合物的结构以及晶胞的计算等,难度不大,注重对基础知识的考查.


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 电负性:④>③>②>① | B. | 原子半径:④>③>②>① | ||
| C. | 第一电离能:④>③>②>① | D. | 最高正化合价:④>③>②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
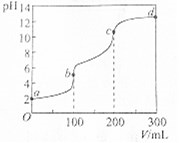 室温下,向100mL一定浓度的草酸(H2C2O4)溶液中加入0.1mol•L-1 NaOH溶液的pH随NaOH溶液体积的变化曲线如图所示.下列有关说法正确的是( )
室温下,向100mL一定浓度的草酸(H2C2O4)溶液中加入0.1mol•L-1 NaOH溶液的pH随NaOH溶液体积的变化曲线如图所示.下列有关说法正确的是( )| A. | a点溶液的pH=2,草酸溶液的浓度为0.005mol•L-1 | |
| B. | b点对应溶液中:c(Na+)>c(HC2O4-)>c(OH-)>c(C2O42-) | |
| C. | b→c段,反应的离子方程式为HC2O4-+OH-═C2O42-+H2O | |
| D. | c→d段,溶液中C2O42-的水解程度逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温常压下为气体 | B. | 不能发生氧化反应 | ||
| C. | 不能自身加成形成聚氯乙烯 | D. | 能使溴的CCl4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
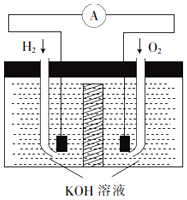 氢氧燃料电池是符合绿色化学理念的新型发电装置.其工作原理如图所示,该电池的电极表面镀了一层细小的铂粉,已知铂吸附气体的能力强,且性质稳定.
氢氧燃料电池是符合绿色化学理念的新型发电装置.其工作原理如图所示,该电池的电极表面镀了一层细小的铂粉,已知铂吸附气体的能力强,且性质稳定.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com