


科目:高中化学 来源: 题型:
| A、分离FeCl3和AlCl3两种物质的混合物,只用氢氧化钠和二氧化碳即可 |
| B、用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 |
| C、稀硫酸滴定未知浓度的NaHCO3溶液,用甲基橙作指示剂,溶液由黄色变为橙色 |
| D、在50mL量筒中配制0.1000mol?L-1碳酸钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| [c(C)]c?[c(D)]d |
| [c(A)]a?[c(B)]b |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(B) |
| c(C) |
查看答案和解析>>
科目:高中化学 来源: 题型:
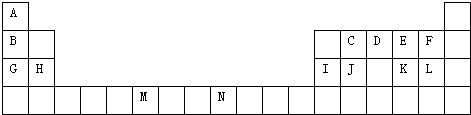
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、根据物质的组成和性质特点,可以将物质分成混合物和纯净物,漂白粉、钢、水玻璃、液氨都为混合物 |
| B、地沟油可用于提炼生物柴油,它和柴油同属于烃类物质 |
| C、大豆蛋白、鸡蛋白分别溶于水所形成的分散系为胶体,在加热、甲醛、饱和(NH4)2SO4溶液、X射线作用下,蛋白质的性质都会改变并发生变性 |
| D、李比希法可用于有机化合物组成中碳、氢元素质量分数的测定,同位素示踪法可用于研究化学反应历程机理 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com