
【题目】某有机物(X)的结构简式如下图,下列关于它的说法不正确的是( )
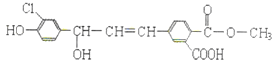
A.X遇FeCl3溶液能发生显色反应
B.一定条件下,X能发生取代、水解、氧化、加成、加聚等反应
C.1mol X分别与足量的NaOH、氢气反应,最多能消耗4mol NaOH 、7mol 氢气
D.等物质的量的该有机物分别与足量的Na、NaHCO3反应时,则消耗Na、NaHCO3的物质的量之比是3:1
【答案】C
【解析】
A.X结构中含酚-OH,遇FeCl3溶液能发生显色反应,故A正确;
B.X结构中含酚-OH、醇-OH、-COOH、-COOC-均可发生取代反应,碳碳双键可发生氧化、加成、加聚反应,-COOC-可发生水解反应,故B正确;
C.含-Cl、酚-OH、-COOH、-COOC-与NaOH反应,苯环、碳碳双键与氢气发生加成反应,则1mol X分别与足量的NaOH、氢气反应,最多能消耗5mol NaOH、7mol氢气,故C错误;
D.酚-OH、醇-OH、-COOH与Na反应,只有-COOH与NaHCO3反应,则与等量X反应时所需Na、NaHCO3的最大量物质的量之比是3:1,故D正确;
答案选C。


科目:高中化学 来源: 题型:
【题目】下图是中学常见物质间的转化关系。已知:
①A为淡黄色固体,B为导致“温室效应”的主要物质; ②E为常见金属,J为红褐色沉淀;
③G在实验室中常用于检验B的存在;④L是一种重要的工业原料,常用于制造炸药,浓溶液常呈黄色,储存在棕色瓶中。
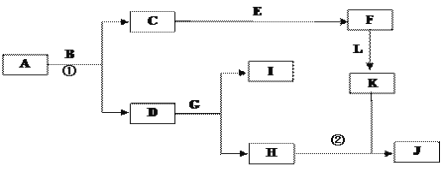
回答下列问题:
(1)A的电子式____________________________________________________。
(2)反应①的化学方程式为__________,反应②的离子方程式为_________________,
(3)若参加反应的A的质量为39g,则消耗CO2的体积(标况下)为__________L。
(4)L的化学式__________,G的化学式__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氧化二铟(In2O3)是一种透明的导电材料,可运用于接触屏、液晶显示器等高科技领域;铟产业被称为“信息时代的朝阳产业”。利用水铟矿[主要成分In(OH)3,常温下Ksp[In(OH)3]=l.41×10-33]制备In2O3的工艺流程如下:
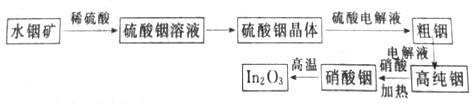
(1)写出水铟矿被硫酸酸浸的离子方程式_____________________________。
(2)从硫酸铟溶液中制备硫酸铟晶体的实验步骤:________、_______、过滤、洗涤、干燥。
(3)某研究机构用硫酸提取铟时,酸度(每升溶液中含硫酸的质量)与浸出率关系如图
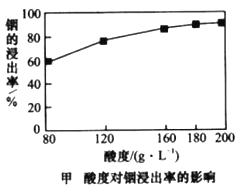
①当酸度为196时,硫酸物质的量浓度为______________。
②请选择适宜的酸度值:___________,并说明选择的理由____________。
(4)完成下列方程式:
(_____)In(NO3)3![]() (_____)In2O3+(_____) _______↑+(_____) _______↑
(_____)In2O3+(_____) _______↑+(_____) _______↑
(5)高纯铟与浓硝酸反应过程中产生的NO2气体可被过氧化钠直接吸收,则标准状况下448mlNO2可被______gNa2O2吸收,NO2的排放会引起一系列的环境问题,任写一条其引起的环境问题___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组利用下图装置探究SO2和Fe(NO3)3溶液的反应原理。其中Na2SO3放在三颈烧瓶中,下列说法不正确的是( )
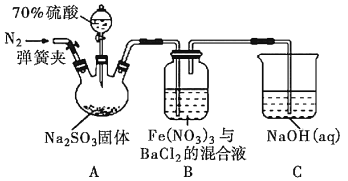
A.装置B中若产生白色沉淀,说明Fe3+能将SO2氧化成SO42-
B.实验室中配制70%的硫酸需要的玻璃仪器有量筒、烧杯、玻璃棒
C.三颈烧瓶中通入N2的操作应在滴加浓硫酸之前,目的是排尽装置内的空气
D.装置C可能发生倒吸,同时还不能完全吸收反应产生的尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验测得:101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ的热量;1 mol CH4完全燃烧生成液态水和CO2,放出890.3 kJ的热量。下列热化学方程式的书写正确的是
①CH4(g)+2O2(g)![]() CO2(g)+2H2O(l) ΔH=+890.3 kJ·mol1
CO2(g)+2H2O(l) ΔH=+890.3 kJ·mol1
②CH4(g)+2O2(g)![]() CO2(g)+2H2O(l) ΔH=890.3 kJ·mol1
CO2(g)+2H2O(l) ΔH=890.3 kJ·mol1
③CH4(g)+2O2(g)![]() CO2(g)+2H2O(g) ΔH=890.3 kJ·mol1
CO2(g)+2H2O(g) ΔH=890.3 kJ·mol1
④2H2(g)+O2(g)![]() 2H2O(l) ΔH=571.6 kJ·mol1
2H2O(l) ΔH=571.6 kJ·mol1
A. 仅有② B. 仅有②④ C. 仅有②③④ D. 全部符合要求
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X溶液中只可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的一种成几种,取该溶液进行实验,实验内容和相关数据
中的一种成几种,取该溶液进行实验,实验内容和相关数据![]() 气体体积在标准状况下测定
气体体积在标准状况下测定![]() 如下:
如下:
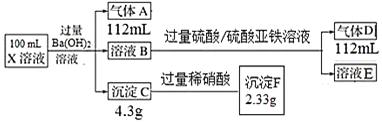
![]() 溶液中一定不存在的离子是______。
溶液中一定不存在的离子是______。
![]() 已知气体D为NO,加入过量
已知气体D为NO,加入过量![]() 和
和![]() 溶液时,发生反应的离子方程式为______。
溶液时,发生反应的离子方程式为______。
![]() 溶液中
溶液中![]() ______
______![]() ,
,![]() ______
______![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁的氧化物成分不一样,性质也不一样, H2还原Fe2O3,发现温度不同,产物也不同。
(1)往产物中滴加盐酸,观察到有气泡产生,生成气泡主要成分的电子式是________。
(2)再滴加KSCN溶液,可观察到________,所得溶液中一定含有的铁的化合价是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅及其化合物是带来人类文明的重要物质![]() 下列说法正确的是
下列说法正确的是![]()
![]()
A.某硅酸盐的化学式为![]() ,可用
,可用![]() 表示
表示
B.水玻璃是纯净物,可用于生产黏合剂和防火剂
C.陶瓷、水晶、水泥、玻璃都属于硅酸盐
D.高纯硅可用于制造光导纤维,高纯二氧化硅可用于制造太阳能电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是一种新型的绿色能源,又是一种重要的化工原料。
(1)氢气燃烧热值高。实验测得,在常温常压下,1gH2完全燃烧生成液态水,放出142.9kJ热量。则H2燃烧的热化学方程式为_____
(2)氢气是合成氨的重要原料,合成氨反应的热化方程式如下:N2(g)+3H2(g)![]() 2NH3(g);ΔH=-92.4kJ/mol
2NH3(g);ΔH=-92.4kJ/mol
①一定条件下,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如图所示,其中加入催化剂引起反应速率变化的时间段是____(填,如0~t1等)。

②生产中为提高反应速率和H2的转化率,下列措施可行的是___(填字母)。
A.向装置中充入过量N2 B.及时将合成的氨气从装置中分离出来
C.使用更高效的催化剂 D.升高温度
③温度为T℃时,将2amolH2和amolN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%。则反应的平衡常数为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com