
| ĪļÖŹ | Ķā¹Ū | ČŪµć | Č¼ÉÕČČ/£ØkJ•mol-1£© |
| ½šøÕŹÆ | ĪŽÉ«£¬ĶøĆ÷¹ĢĢå | £æ | 395.4 |
| ŹÆÄ« | »ŅŗŚ£¬²»ĶøĆ÷¹ĢĢå | £æ | 393.5 |
| A£® | ÓɱķÖŠŠÅĻ¢æɵĆČēÓŅĶ¼ĖłŹ¾µÄĶ¼Ļó | |
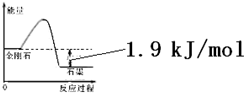
| B£® | ÓɱķÖŠŠÅĻ¢ÖŖC£ØŹÆÄ«£¬s£©=C£Ø½šøÕŹÆ£¬s£©”÷H=+1.9kJ/mol | |
| C£® | ÓɱķÖŠŠÅĻ¢æÉĶĘÖŖĻąĶ¬Ģõ¼žĻĀ½šøÕŹÆµÄČŪµćµĶÓŚŹÆÄ«µÄČŪµć | |
| D£® | ±ķŹ¾ŹÆÄ«Č¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½ĪŖC£ØŹÆÄ«£¬s£©+$\frac{1}{2}$O2£Øg£©=CO£Øg£©”÷H=-393.5kJ/mol |
·ÖĪö A£®Ķ¼ĻóÖŠ½šøÕŹÆ±ä»ÆĪŖŹÆÄ«ŹĒ·ÅČČ·“Ó¦£¬·Å³öČČĮæĪŖ½šøÕŹÆŗĶŹÆÄ«Č¼ÉÕČČÖ®²ī£»
B£®ŅĄ¾ŻøĒĖ¹¶ØĀÉ£¬½įŗĻ½šøÕŹÆŗĶŹÆÄ«Č¼ÉÕČČ¼ĘĖćµĆµ½£»
C£®ŹÆÄ«µÄ²ćÄŚ¹²¼Ū¼ü¼ü³¤±Č½šøÕŹÆµÄ¼ü³¤¶Ģ£¬×÷ÓĆĮ¦øü“ó£¬ĘĘ»µ»Æѧ¼üŠčŅŖøü“óÄÜĮ棬ĖłŅŌŹÆÄ«µÄČŪµć±Č½šøÕŹÆøߣ»
D£®ŅĄ¾ŻČ¼ÉÕČČŹĒ1molæÉČ¼ĪļĶźČ«Č¼ÉÕÉś³ÉĪȶØŃõ»ÆĪļ·Å³öµÄČČĮæ·ÖĪö£®
½ā“š ½ā£ŗA£®Ķ¼ĻóÖŠ1.9kJ/mol£¬ŹĒ½šøÕŹÆŗĶŹÆÄ«ÄÜĮæ²ī£¬¹ŹAÕżČ·£»
B£®ÓɱķÖŠŠÅĻ¢ÖŖ£¬½šøÕŹÆČ¼ÉÕČČ395.4KJ/mol£¬ŹÆÄ«Č¼ÉÕČČ393.5KJ/mol£¬C£ØŹÆÄ«£¬s£©ØTC£Ø½šøÕŹÆ£¬s£©”÷H=+1.9 kJ•mol£¬¹ŹBÕżČ·£»
C£®µČĪļÖŹµÄĮ潚øÕŹÆŗĶŹÆÄ«Ļą±Č£¬ŹÆÄ«ÄÜĮæµĶÓŚ½šøÕŹÆ£¬ÄÜĮæŌ½µĶŌ½ĪČ¶Ø£¬ŹÆÄ«µÄ²ćÄŚ¹²¼Ū¼ü¼ü³¤±Č½šøÕŹÆµÄ¼ü³¤¶Ģ£¬×÷ÓĆĮ¦øü“ó£¬ĘĘ»µ»Æѧ¼üŠčŅŖøü“óÄÜĮ棬ĖłŅŌŹÆÄ«µÄČŪµć±Č½šøÕŹÆøߣ¬¹ŹCÕżČ·£»
D£®±ķŹ¾ŹÆÄ«Č¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½ĪŖC£ØŹÆÄ«£¬s£©+O2£Øg£©ØTCO2£Øg£©”÷H=-393.5 kJ•mol-1£¬¹ŹD“ķĪó£¬
¹ŹŃ”D£®
µćĘĄ ±¾ĢāÖ÷ŅŖæ¼²éµÄŹĒČ¼ÉÕČČøÅÄī·ÖĪöŅŌ¼°½šøÕŹÆÓėŹÆÄ«µÄĻą»„×Ŗ»Æ”¢Ķ¼Ļó·ÖĪö·½·ØÓ¦ÓĆ£¬ÕĘĪÕ»ł“”£¬Ąķ½āŹµÖŹŹĒ¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 22.4LČĪŗĪĘųĢåµÄĪļÖŹµÄĮæ¾łĪŖ1mol | |
| B£® | ±ź×¼×“æöĻĀ£¬1molĪļÖŹµÄĢå»żĪŖ22.4L | |
| C£® | H2”¢O2”¢N2”¢CO2×é³ÉµÄ»ģŗĻĘųĢå1molŌŚ±ź×¼×“æöĻĀµÄĢå»żŌ¼ĪŖ22.4L | |
| D£® | ŌŚĶ¬ĪĀĶ¬Ń¹ĻĀ£¬ĻąĶ¬Ģå»żµÄČĪŗĪĘųĢåµ„ÖŹĖłŗ¬·Ö×ÓŹżŗĶŌ×ÓŹż¶¼ĻąĶ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H2O | B£® | NH3•H2O | C£® | CH3COOH | D£® | NaCl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
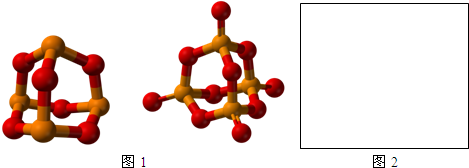
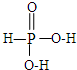 £¬Š“³öH3PO2Óė×ćĮæĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦µÄ»Æѧ·½³ĢŹ½NaOH+H3PO2=Na H2PO2+H2O£®Į×µÄČżÖÖŗ¬ŃõĖįH3PO2”¢H3PO3”¢H3PO4µÄĖįŠŌĒæČõĖ³ŠņĪŖH3PO2£¼H3PO3£¼H3PO4£¬ĘäŌŅņŹĒH3PO2”¢H3PO3”¢H3PO4ÖŠĮ×ŌŖĖŲµÄ»ÆŗĻ¼ŪŅĄ“ĪĪŖ+1£¬+3ŗĶ+5¼Ū£¬ÖŠŠÄĮ×Ō×ÓµÄÕżµēŗÉŅĄ“ĪÉżøߣ¬µ¼ÖĀP-O-HÖŠOµÄµē×ÓøüŅ×ĻņPĘ«ŅĘ£¬Ņņ¶ųH3PO2”¢H3PO3”¢H3PO4Ō½Ņ×µēĄė³öĒāĄė×Ó£¬ĖįŠŌŌ½Ą“Ō½Ē森
£¬Š“³öH3PO2Óė×ćĮæĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦µÄ»Æѧ·½³ĢŹ½NaOH+H3PO2=Na H2PO2+H2O£®Į×µÄČżÖÖŗ¬ŃõĖįH3PO2”¢H3PO3”¢H3PO4µÄĖįŠŌĒæČõĖ³ŠņĪŖH3PO2£¼H3PO3£¼H3PO4£¬ĘäŌŅņŹĒH3PO2”¢H3PO3”¢H3PO4ÖŠĮ×ŌŖĖŲµÄ»ÆŗĻ¼ŪŅĄ“ĪĪŖ+1£¬+3ŗĶ+5¼Ū£¬ÖŠŠÄĮ×Ō×ÓµÄÕżµēŗÉŅĄ“ĪÉżøߣ¬µ¼ÖĀP-O-HÖŠOµÄµē×ÓøüŅ×ĻņPĘ«ŅĘ£¬Ņņ¶ųH3PO2”¢H3PO3”¢H3PO4Ō½Ņ×µēĄė³öĒāĄė×Ó£¬ĖįŠŌŌ½Ą“Ō½Ē森²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.5molµÄK+ | B£® | 0.5molµÄH+ | C£® | 1.0molµÄH+ | D£® | 1.0molµÄOH- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | $\frac{22.4}{Vn}$ | B£® | $\frac{22.4n}{V}$ | C£® | $\frac{Vn}{5.6}$ | D£® | $\frac{5.6n}{V}$ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | “ż¼ģŅŗ¼ÓČėĀČ»Æ±µČÜŅŗÓŠ°×É«³ĮµķÉś³É£¬ŌŁ¼ÓČėŃĪĖį³ĮµķĻūŹ§ĒŅ²śÉśĪŽÉ«ĪŽĪ¶µÄĘųĢ壬Ōņ“ż¼ģŅŗÖŠŅ»¶Øŗ¬ÓŠCO32- | |
| B£® | ¼ÓČėĀČ»Æ±µČÜŅŗÓŠ°×É«³ĮµķÉś³É£¬ŌŁ¼ÓĻ”ĻõĖį£¬³Įµķ²»ĻūŹ§£¬Ņ»¶Øŗ¬ÓŠSO42- | |
| C£® | ½«ĒāĘųŌŚÄ³ĘųĢåÖŠµćČ¼£¬Čō²śÉś²Ō°×É«»šŃę£¬ŌņøĆĘųĢåĪŖĀČĘų | |
| D£® | “ż¼ģŅŗ¼ÓČėNaOHČÜŅŗ²¢¼ÓČČ£¬ÓŠÄÜŹ¹ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½±äĄ¶µÄĘųĢåÉś³É£¬ŌņŌČÜŅŗÖŠŅ»¶Øŗ¬ÓŠNH4+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČČĪČ¶ØŠŌ£ŗNa2CO3£¼NaHCO3 | |
| B£® | ¼īŠŌ£ŗNa2CO3£¼NaHCO3 | |
| C£® | Ė®ÖŠµÄČܽā¶Č£ŗNa2CO3£¾NaHCO3 | |
| D£® | Óė×ćĮæµÄŃĪĖį·“Ó¦²śÉśµÄĘųĢåµÄĢå»ż£ŗNa2CO3£¼NaHCO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2.7 mol/L | B£® | 1.35 mol/L | C£® | 0.9 mol/L | D£® | 0.45 mol/L |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com