
| A. | 羟基的电子式 | B. | 二氧化硅的结构式 O=Si=O | ||
| C. | NH3的球棍模型 | D. | X=11,图表示钠原子的结构示意图 |
分析 A.羟基由一个氧原子和一个氢原子构成,氧原子最外层6个电子,氢原子最外层一个电子,二者形成一个共用电子对;
B.二氧化硅为原子晶体,晶体中不存在硅氧双键;
C.氨气为三角锥的空间构型,选项中为比例模型;
D.钠原子核内有11个质子,核外有3个电子层,最外层上有1个电子.
解答 解;A.羟基由一个氧原子和一个氢原子构成,氧原子最外层6个电子,氢原子最外层一个电子,二者形成一个共用电子对,所以羟基的电子式是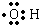 ,故A正确;
,故A正确;
B.由于二氧化硅为原子晶体,1个硅原子形成4个硅氧键,1个氧原子形成2个硅氧键,所以二氧化硅中不存在硅氧双键,故B错误;
C.氨气为三角锥的空间构型,故氨气的球棍模型为 ,故C错误;
,故C错误;
D.钠原子核内有11个质子,核外有3个电子层,第一层上有2个电子、第二层上有8个电子,最外层上有1个电子,其原子结构示意图为: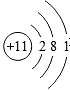 ,故D错误;
,故D错误;
故选A.
点评 本题考查常用化学用语,涉及电子式、结构示意图、结构式、球棍模型等,题目难度不大,注意羟基为中性原子团.


科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2+HCl $\stackrel{催化剂}{→}$CH3CH2Cl 加聚反应 | |
| B. | CH3COOCH2CH3+NaOH→CH3COONa+CH3CH2OH 取代反应 | |
| C. |  +Br2$\stackrel{FeBr_{3}}{→}$ +Br2$\stackrel{FeBr_{3}}{→}$ +HBr 加成反应 +HBr 加成反应 | |
| D. |  +HNO3$→_{50~60℃}^{浓H_{2}SO_{4}}$ +HNO3$→_{50~60℃}^{浓H_{2}SO_{4}}$ +H2O 取代反应 +H2O 取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  用图制备Fe(OH)2 | B. |  用图制备少量Cl2 | ||
| C. |  用图制备并收集O2 | D. |  用图比较S、C、Si的非金属性强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 非金属及其化合物在工农业生产、生活中有着重要应用,减少非金属的氧化物在大气中的排放是环境保护的重要内容之一.
非金属及其化合物在工农业生产、生活中有着重要应用,减少非金属的氧化物在大气中的排放是环境保护的重要内容之一.| t/min | 0.00 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 |
| c(N2O5)/(mo•L-1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2 和 H2O | B. | CO 和 CH3OH | C. | CH3OH 和 H2 | D. | H2 和 CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 电流表指针不会发生偏转 | B. | 除去锌镀层的铁片为负极 | ||
| C. | 负极的电极反应式:Fe-2e→Fe2+ | D. | 锌镀层反应完毕后电流计指针归零 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当n=2时,物质A、B的转化率之比为1:2 | |
| B. | 起始时刻和达到平衡后容器中的压强比为(1+n):(l+n-$\frac{a}{2}$) | |
| C. | 当v (A)正=2v (C)逆时,可断定反应达到平衡 | |
| D. | 容器中混合气体的密度不再随时间改变而改变,反应到达平衡状态 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com