
| n |
| V |
| n |
| V |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ܵ���ʵ��ܶȻ�ԽС���ܽ��Խ�� |
| B��һ��Ũ�ȵ�NH4Cl��Һ�����ܽ�Mg��OH��2 |
| C�������¶ȣ����ʵ��ܽ�ȶ������� |
| D������ͨ��������Ӧʹ����������ȫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����������ӵĺ�������Ų���ȫ��ͬ����ѧ����һ����ͬ |
| B�������ԭ�ӵĺ�������Ų���ͬ����һ������ͬһ��Ԫ�� |
| C���������Ԫ�صĻ�����һ������ǿ������ |
| D��������ֻ�ܵõ��ӱ���ԭ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ϡHNO3�ܽ�FeS���壺FeS+2H+=Fe2++H2S�� |
| B������ͨ�����ʯ��ˮ�У�Cl2+2OH-=Cl-+ClO-+H2O |
| C����С�մ�����θ����ࣺCO32-+2H+=CO2��+H2O |
| D����������Һ��ͨ�����������̼��SiO32-+CO2+H2O=H2SiO3��+CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


| hv |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
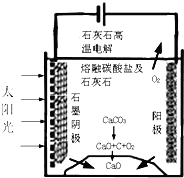 ��Դ�����ö�����̼�����ɼ�������������ŷţ��������»��ȼ�ϻ���Ҫ��ҵ��Ʒ��
��Դ�����ö�����̼�����ɼ�������������ŷţ��������»��ȼ�ϻ���Ҫ��ҵ��Ʒ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� |
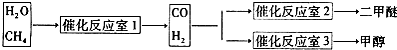

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com