
| ||
| ||


科目:高中化学 来源: 题型:
| A、在常温常压下,11.2LN2含有的分子数为0.5NA |
| B、在常温常压下,1mol氦气含有的原子数为2NA |
| C、71gCl2所含原子数为2NA |
| D、23g钠在化学反应中失去电子数目为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、单质硅是将太阳能转化为电能的常用材料 |
| B、硅酸钠的俗名为玻璃,可用于制备硅胶和木材防火剂 |
| C、用浓H2SO4刻蚀工艺玻璃上的纹饰 |
| D、SO2具有氧化性,可用来漂白纸浆 |
查看答案和解析>>
科目:高中化学 来源: 题型:
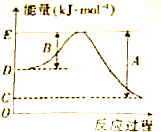 下表列出了断裂某些化学键的热量值
下表列出了断裂某些化学键的热量值| 化学键 | H-H | Cl-Cl | I-I | O═O | C-Cl | C-H | O-H | H-Cl | H-I |
| 断裂1mol化学键所吸收的能量(kJ) | 436 | 247 | 151 | x | 330 | 413 | 463 | 431 | 299 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 实验内容 | 试剂 | 实验现象 |
| 验证氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
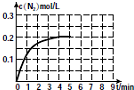 研究化学反应,不仅要关注反应的速率、方向性,还要关注反应进行的限度以及反应过程中的能量变化.
研究化学反应,不仅要关注反应的速率、方向性,还要关注反应进行的限度以及反应过程中的能量变化.| 0 | 1min | 2min | 4min | 5min | |
| 130℃ | 0.50mol | 0.35mol | 0.25mol | 0.10mol | 0.10mol |
| 180℃ | 0.50mol | 0.30mol | 0.18mol | 0.15mol |
| c2(N2)?c2(H2O) |
| c2(NH3)?c(NO)?c(NO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO和SiO2都不能和水反应,所以它们都不是酸性氧化物 |
| B、易溶于水的化合物溶于水的过程不一定有化学键断裂的过程 |
| C、Na2O2是离子化合物,含有极性键和离子键 |
| D、氢氧化铝是两性氢氧化物,既可溶解于浓氨水又可溶解于盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com