
【题目】选择一种容积将溴水中的溴萃取出来,这种溶剂应该具有的性质
A.易溶于水,且不与溴发生反应 B.不溶于水,且密度必须比水小
C.不溶于水,且密度必须比水大 D.不溶于水,且比水更容易使溴溶解
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在同温、同压下,A容器的氮气和B容器的氨气中,若它们所含的原子数相等,则这两个容器的体积之比是
A.2:1 C.2:3 B.1:2 D.1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】味精(主要成分的化学式为C5H8NO4 Na·H2O)中往往含少量食盐,某学生想测定某品牌味精的纯度,做了如下实验:
①称取某品牌的袋装味精样品1.000 g,放入烧杯中,加入蒸馏水溶解,恢复至室温;
②在烧杯中,加入稍过量的用稀硝酸酸化的A溶液,充分反应,使沉淀完全;
③过滤,用蒸馏水反复洗涤沉淀多次;
④将沉淀烘干、称量,所得固体质量为0.368 g。
根据上述实验操作,回答下列问题:
(1)加入的A溶液是________;检验加入的A溶液是否过量的方法是_______________________。
(2)沉淀洗涤是必不可少的一步,若沉淀不洗涤,测得的结果将_____________。
(3)烘干沉淀应采用的方法是________(填字母)。
A.低温烘干 B.高温烘干 C.利用太阳能晒干
(4)该品牌味精的纯度(即味精中C5H8NO4 Na·H2O的质量分数)为__________。
(5)写出味精和食盐中都含有的元素的离子结构示意图:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分类是学习化学的方法之一,下列各组物质按氧化物、酸、碱、盐顺序排列的一组是( )
A.氢氧化铁、硝酸、烧碱、氯化钠
B.干冰、碳酸、纯碱、硫酸钾
C.水、硫酸、熟石灰、氯化钾
D.氨水、醋酸、氢氧化铁、食盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:在常温下,苯(C6H6)为一种无色、透明的液体,毒性较高,易挥发,易燃,有腐蚀性,沸点为80.1℃,难溶于水,易溶于有机溶剂,可作为有机溶剂;碘(I2)为紫黑色晶体,易升华,易凝华,熔点113.5℃,沸点184.3℃,加热时碘升华为紫色蒸气,冷却后凝华成紫黑色固体。实验室常用苯来提取碘水中的碘,具体操作如下:
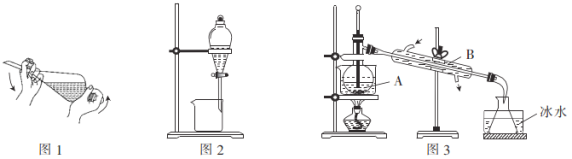
①向碘的水溶液中加入萃取剂苯,转移到分液漏斗中,塞上玻璃塞,充分振荡放气后(如图1);
②将分液漏斗置于铁架台的铁圈上静置(如图2);
③当分液漏斗中的液体分成清晰的两层后,经“合适的操作”将两层液体进行分离;
④将分离出的碘和苯的混合液转移到仪器A中,加入少量沸石进行蒸馏以分离苯和碘(如图3)。
请回答下列问题:
(1)分液漏斗在使用前必须进行的操作是_______;振荡静置后溶有碘的苯溶液在分液漏斗的_____(填“上层”或“下层”)。
(2)步骤③中“合适的操作”的名称是________。
(3)步骤④中采用水浴加热而不直接加热的原因是________________;图3中仪器A的名称是______;图3中有多处明显的错误:a.冷却水进出方向错误.b.____________;C.___________。
(4)锥形瓶置于冰水中的目的是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SiO2广泛存在于自然界中,其在工业生产中有着广泛的用途。
(1)白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在一定条件下反应获得。相关热化学方程式如下:
2Ca3(PO4)2(s)+10C(s)==6CaO(s)+P4(s)+10CO(g) ΔH1=+3 359.26 kJ·mol-1
CaO(s)+SiO2(s)==CaSiO3(s) ΔH2=-89.61 kJ·mol-1
2Ca3(PO4)2(s)+6SiO2(s)+10C(s)==6CaSiO3(s)+P4(s)+10CO(g) ΔH3 则ΔH3=________ kJ·mol-1。
(2)工业上用石英砂和焦炭可制得粗硅。
已知:
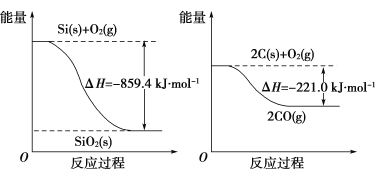
请将以下反应的热化学方程式补充完整:
SiO2(s)+2C(s)==Si(s)+2CO(g) ΔH=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是( )
A. 18 g H2O中含有10NA个质子
B. 1 mol甲苯中含有6NA个C—H键
C. 标准状况下,22.4 L氨水中含有NA个NH3分子
D. 将56 g铁片投入足量浓H2SO4中生成NA个SO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探讨浓度对化学平衡的影响,某同学对可逆反应 “2Fe3++2I-![]() 2Fe2++I2 △H<0”按下图所示步骤进行了一系列实验。
2Fe2++I2 △H<0”按下图所示步骤进行了一系列实验。

说明:0.005 mol·L-1的Fe2(SO4)3溶液颜色接近于无色。
(1)实验中要待实验Ⅰ溶液颜色不再改变时,才能进行实验Ⅱ,目的是 。
(2)实验Ⅱ中,ⅰ的现象是 ,该实验证明 。
(3)实验Ⅱ中,ⅲ的化学平衡向 移动(填“正反应方向”或“逆反应方向”);ⅲ的现象是溶液变浅,该现象 (填“能”或“不能”)说明化学平衡发生移动。如果前一空填“能”,则下一空不填;如果前一空填“不能”,则ⅲ的目的是 。
(4)实验Ⅱ中,ⅱ的现象是 ,即能证明增大生成物浓度化学平衡发生了逆向移动。
(5)除了上图中的方法外,若要使该可逆反应的化学平衡逆向移动,还可以采用的方法有 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.5L 2mol/L FeCl3溶液与0.2L 5mol/L KCl溶液中的Cl﹣物质的量之比( )
A.6:5
B.3:2
C.15:2
D.3:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com