
分析 (1)还原性:Fe2+>Br-,氯气先氧化Fe2+,再氧化Br-;
(2)二氧化碳过量,偏铝酸钠溶液与二氧化碳反应生成了氢氧化铝和碳酸氢钠;
(3)Ba(OH)2溶液中加入足量NaHCO3反应生成碳酸钡和碳酸钠;
(4)过氧化钠具有强氧化性,氯化亚铁与过氧化钠反应生成氢氧化铁沉淀、氯化钠和氯化铁;
(5)向碳酸氢钠和碳酸钠的混合溶液中通入过量的二氧化碳,碳酸钠、二氧化碳和水反应生成碳酸氢钠.
解答 解:(1)因还原性:Fe2+>Br-,氯气先氧化Fe2+,再氧化Br-,向FeBr2溶液中通入少量Cl2,只发生Cl2+2Fe2+═2Fe3++2Cl-,
故答案为:Cl2+2Fe2+═2Fe3++2Cl-;
(2)偏铝酸钠溶液中通入过量二氧化碳,反应生成了氢氧化铝沉淀和碳酸氢钠,反应的离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,
故答案为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
(3)Ba(OH)2溶液中加入足量NaHCO3反应生成碳酸钡和碳酸钠,反应的离子方程式为:Ba2++2HCO3-+2OH-=BaCO3↓+2H2O+CO32-,故答案为:Ba2++2HCO3-+2OH-=BaCO3↓+2H2O+CO32-;
(4)过氧化钠具有强氧化性,氯化亚铁与过氧化钠反应生成氢氧化铁沉淀、氯化钠和氯化铁,反应的化学方程式:3Na2O2+6Fe2++6H2O=2Fe3++4Fe(OH)3↓+6Na+,故答案为:3Na2O2+6Fe2++6H2O=2Fe3++4Fe(OH)3↓+6Na+;
(5)向碳酸氢钠和碳酸钠的混合溶液中通入过量的二氧化碳,碳酸钠、二氧化碳和水反应生成碳酸氢钠,反应为CO32-+CO2+H2O=2HCO3-,
故答案为:CO32-+CO2+H2O=2HCO3-.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应及与量有关的离子反应的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
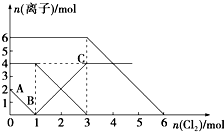 已知:2Fe2++Br2═2Fe3++2Br-,2Fe3++2I-═2Fe2++I2.向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.下列有关说法中,不正确的是( )
已知:2Fe2++Br2═2Fe3++2Br-,2Fe3++2I-═2Fe2++I2.向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.下列有关说法中,不正确的是( )| A. | 还原性:I->Fe2+>Br- | |
| B. | 原混合溶液中FeBr2的物质的量为6 mol | |
| C. | 当通入2 mol Cl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- | |
| D. | 原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
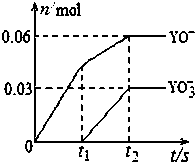 有关元素X、Y、Z、D、E的信息如下
有关元素X、Y、Z、D、E的信息如下| 元素 | 有关信息 |
| X | 元素主要化合价为-2,原子半径为0.074nm |
| Y | 所在主族序数与所在周期序数之差为4 |
| Z | 原子半径为0.102nm,核外最外层电子数是其电子层数的2倍,其单质在X的单质中燃烧,产生的气体通入品红中,品红褪色. |
| D | 最高价氧化物对应的水化物,是强电解质,能电离出电子数相等的阴、阳离子 |
| E | 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
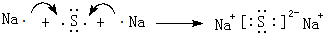 ,D2Z水溶液显碱性,用离子方程式表示其原因S2-+H2O?HS-+OH-
,D2Z水溶液显碱性,用离子方程式表示其原因S2-+H2O?HS-+OH-查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-甲基-2-丁烯 | B. | 2-乙基丙烷 | ||
| C. | 3-甲基-2-丁烯 | D. | 2,2-二甲基-3-戊炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最外层有3个未成对电子的原子 | B. | 最外层电子排布为ns2的原子 | ||
| C. | 次外层无未成对电子的原子 | D. | 最外层有8个电子的原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(OH-)=10-12 mol/L的溶液:K+、Ba2+、Cl-、Br - | |
| B. | 滴加甲基橙试剂显红色的溶液中:Na+、Fe2+、Cl-、NO3- | |
| C. | c(OH-)/c(H+)=1012的溶液中:NH4+、Al3+、NO3-、CO32- | |
| D. | 由水电离的c(H+)=1.0×10-13 mol/L的溶液中:K+、NH4+、AlO2-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 互为手性异构体的分子具有完全相同的组成和原子排列 | |
| B. | H2O是一种非常稳定的化合物,这是由于氢键所致 | |
| C. | 冰晶体具有空间网状结构,是原子晶体 | |
| D. | 非极性分子中,各原子间都应以非极性键结合 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com