

| A. | 制取Fe(OH)2的装置及操作 | |
| B. | 某溶液用盐酸酸化后再滴加硝酸钡溶液,检验溶液中是否含有SO42- | |
| C. | 向滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后溶液的红色褪去,可证明Na2CO3溶液显碱性是由于CO32-水解造成的 | |
| D. | 将氯化铁饱和滚液与稀氨水混合,加热至沸腾,制备Fe(OH)3胶体 |
分析 A.氢氧化亚铁易被空气中氧气氧化,图示操作无法制取氢氧化亚铁;
B.硝酸根离子在酸性条件下能够氧化二氧化硫,应该滴加氯化钡溶液;
C.碳酸钠溶液水解显示碱性,碳酸根离子可以和钡离子反应生成碳酸钡沉淀;
D.氯化铁与氨水反应生成氢氧化铁沉淀,无法获得胶体.
解答 解:A.Fe(OH)2易被氧化,制取Fe(OH)2时应该在氯化亚铁溶液表明滴加一层植物油,然后将胶头滴管下端插入氯化亚铁溶液中,故A错误;
B.某溶液用盐酸酸化后再滴加硝酸钡溶液,由于二氧化硫易溶于水,酸性条件下硝酸根离子能够将二氧化硫氧化成硫酸,干扰了检验结果,应该滴加氯化钡溶液,故B错误;
C.Na2CO3为强碱弱酸盐,水解呈碱性,加入氯化钡生成碳酸钡沉淀,水解程度减小,可证明Na2CO3溶液显碱性是由于CO32-水解造成的,故C正确;
D.将氯化铁饱和滚液与稀氨水混合,得到的是氢氧化铁沉淀,无法制备Fe(OH)3胶体,故D错误;
故选C.
点评 本题考查了化学实验方案的评价,题目难度中等,涉及氢氧化亚铁、氢氧化铁胶体制备、盐的水解原理、离子检验等知识,明确常见化学实验基本操作方法即可解答,试题有利于提高学生的分析能力及化学实验能力.


 全能练考卷系列答案
全能练考卷系列答案科目:高中化学 来源: 题型:选择题
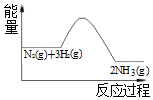
| A. | 反应体系中加入催化剂,不会改变反应的热效应 | |
| B. | 反应物的总能量高于生成物的总能量 | |
| C. | 该反应的热化学方程式为 3H2+N2?2NH3+Q(Q>0) | |
| D. | 该反应是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
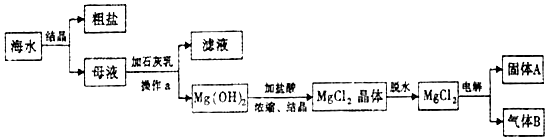
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
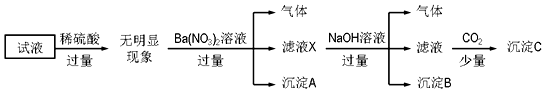
| A. | 原溶液中存在的离子为NH4+、Fe2+、Cl-、SO42- | |
| B. | 滤液X中大量存在的阳离子有NH4+、Fe2+和Ba2+ | |
| C. | 沉淀C为Al(OH)3 | |
| D. | 无法确定原试液中是否含有K+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | (CH3)2CHCH2CH3 2-甲基丙烷 | B. | (CH3)2C=CHCH3 2-甲基-2-丁烯 | ||
| C. |  2-丁烯 2-丁烯 | D. |  1,4-二甲苯 1,4-二甲苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
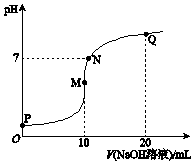 25℃时,向10mL 0.1mol•L-1 NH4HSO4溶液中逐滴滴入0.1mol•L-1 NaOH溶液,溶液的pH与NaOH溶液体积关系如图所示.下列选项正确的是( )
25℃时,向10mL 0.1mol•L-1 NH4HSO4溶液中逐滴滴入0.1mol•L-1 NaOH溶液,溶液的pH与NaOH溶液体积关系如图所示.下列选项正确的是( )| A. | P点pH较低的主要原因是NH4+水解 | |
| B. | P、M、N、Q四点中,水的电离程度较大的是N点 | |
| C. | M点 c(Na+)>c(NH4+); N点 c(NH4+)+c(Na+)═2c(SO42-) | |
| D. | Q点 c(NH4+)+c(NH3•H2O)═c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
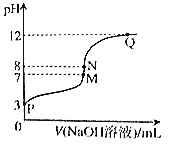 T℃时,在20.00mL0.10mol•L-1CH3COOH溶液中滴入0.10mol•L-1NaOH溶液,溶液pH与NaOH溶液体积关系关系如图所示.下列说法正确的是( )
T℃时,在20.00mL0.10mol•L-1CH3COOH溶液中滴入0.10mol•L-1NaOH溶液,溶液pH与NaOH溶液体积关系关系如图所示.下列说法正确的是( )| A. | T℃时,CH3COOH电离平衡常数Ka=1.0×10-3 | |
| B. | M点对应的NaOH溶液体积为20.00mL | |
| C. | N点与Q点所示溶液中水的电离程度:N>Q | |
| D. | N点所示溶液中c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com