
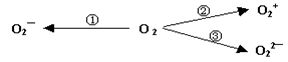
| A.O4分子内存在极性共价键 |
| B.合成O4的反应不属于化学变化 |
| C.O4与O3、O2都是氧的同素异形体 |
| D.O4将来可用作更强有力的火箭推进的氧化剂 |
 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源:不详 题型:单选题
| 化学键 | H—H | H—Cl | H—I | Cl—Cl | Br—Br |
| 键能/ kJ/mol | 436 | 431 | 299 | 247 | 193 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②⑤ | B.①⑤ | C.⑤ | D.③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
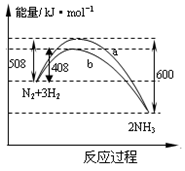
A.该反应的热化学方程式为:1/2 N2(g)+3/2 H2(g) NH3(g) △H= -92kJ·mol-1 NH3(g) △H= -92kJ·mol-1 |
| B.不用催化剂,生成 1molNH3放出的热量为46 KJ |
| C.加入催化剂,生成 1molNH3的反应热减小50 KJ·mol-1 |
| D.曲线b表明加入催化剂降低了反应热,加快了反应速率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.碘的升华 | B.氯化钠溶于水 | C.氯化氢溶于水 | D.氯化铵受热分解。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.工业上制氨气的反应 | B.葡萄糖在人体内氧化分解 |
| C.锌粒与稀H2SO4反应制取H2 | D.Ba(OH)2·8H2O与NH4Cl反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com