
| 1 | 操作 | 现象 | 结 论 |
| A | 向白色AgCl悬浊液中滴加0.1mol/LKI溶液 | 试管中白色沉淀转化为黄色沉淀. | Ksp(AgCl)>Ksp(AgI) |
| B | 向装有Fe(NO3)2溶液的试管中加入几滴稀H2SO4 | 溶液颜色基本不变 | Fe(NO3)2与H2SO4不反应 |
| C | 向Na2SiO3溶液中滴加盐酸 | 溶液变浑浊 | 非金属性:Cl>Si |
| D | SO2通入足量的稀Fe(NO3)3溶液 | 溶液由棕黄色变为浅绿色,后立即又变成棕黄色 | 氧化性:HNO3>H2SO4>Fe3+ |
| A. | A | B. | B | C. | C | D. | D |
分析 A.溶度积大的物质能转化为溶度积小的物质;
B.酸性条件下,硝酸根离子具有强氧化性;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸;
D.同一氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性.
解答 解:A.发生沉淀导的转化,向溶度积更小的方向移动,则向新制的AgCl乳白色悬浊液中滴加0.1mol/L的KI溶液,产生黄色沉淀,证明:Ksp[AgCl]>Ksp[AgI],故A正确;
B.酸性条件下,硝酸根离子具有强氧化性,酸性条件下硝酸根离子将亚铁离子氧化生成铁离子,故B错误;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸,HCl不是Cl元素的最高价氧化物的水化物,所以不能据此判断非金属性强弱,故C错误;
D.同一氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性,由溶液有棕色变为浅绿色,说明三价铁的氧化性强于稀硫酸,但在硝酸存在的前提下立即又变成棕黄色,说明亚铁迅速被氧化成铁离子,故硝酸的氧化性强三价铁,综上所述氧化性:HNO3>Fe3+>稀硫酸,故D错误;
故选A.
点评 本题考查化学实验方案评价,为高频考点,涉及氧化还原反应、非金属性强弱判断、难溶物的转化等知识点,明确实验原理及物质性质是解本题关键,注意挖掘隐含条件,易错选项是C.


科目:高中化学 来源: 题型:多选题
| A. | N2O结构式可表示为N=N=O | |
| B. | O3分子呈直线形 | |
| C. | CH2=CH-CHO分子中碳原子均采用sp2杂化 | |
| D. | 相同压强下,HCOOH沸点比CH3OCH3高,说明前者是极性分子,后者是非极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质(少量杂质) | 操作 | |
| A | KNO3固体(NaCl) | 加水溶解、蒸发结晶、趁热过滤、洗涤、干燥 |
| B | NaCl固体(KNO3) | 加水溶解、蒸发浓缩、冷却结晶、过滤、洗涤、干燥 |
| C | FeCl3溶液(NH4Cl) | 加热蒸干、灼烧 |
| D | NH4Cl溶液(FeCl3) | 滴加氨水至不再产生沉淀为止,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沸点由低到高的顺序为:CH3CH2CH3<CH3(CH2)2CH3<(CH3)3CH | |
| B. | 工业上合成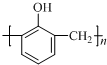 的单体为甲醛和苯酚( 的单体为甲醛和苯酚(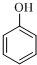 ) ) | |
| C. | 相同质量的乙烯和乙酸完全燃烧时,消耗氧气的量相同 | |
| D. | 某烷烃可以命名为2,3,3-三甲基-4-乙基戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用米汤检验碘盐中的碘 | |
| B. | 用热的烧碱溶液洗涤餐具上的油污 | |
| C. | “地沟油”禁止食用,但可用来制取肥皂 | |
| D. | 将洁厕灵与84消毒液混合使用,能更有效的起到洁具除垢和卫生消毒作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该电池的工作环境应在高温条件下 | |
| B. | 正极反应:O2+2H2O+4e-═4OH- | |
| C. | 电池工作时葡萄糖在负极上失去电子发生还原反应 | |
| D. | 电池工作时H+由负极移向正极,电解质溶液的pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
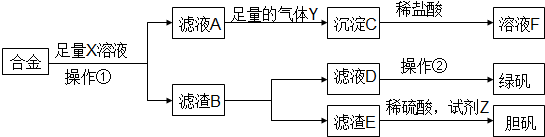
| A. | 溶液X为稀硫酸,气体Y为氨气 | |
| B. | 由溶液F获得溶质F固体的过程中,须控制条件防止其氧化和分解 | |
| C. | 使用足量稀硫酸时,试剂Z选用H2O2或适量HNO3均获得胆矾晶体 | |
| D. | 操作①为过滤,操作②为蒸发结晶、洗涤、干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| Q | X | ||
| Y | Z | W | |
| T |
| A. | X、Z、Y元素的原子半径及它们的气态氢化物的热稳定性均依次递增 | |
| B. | Y、Z、W元素在自然界中均能以游离态存在,它们的最高价氧化物的水化物的酸性依次递增 | |
| C. | Q与氢元素形成的化合物中不存在非极性共价键 | |
| D. | 根据元素周期律,可以推测T元素的单质具有半导体特性,最高价氧化物对应水化物的化学式是H3TO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com