
【题目】25℃时,0.1mol Na2CO3与盐酸混合所得溶液的体积为1L,溶液中部分微粒浓度与pH 的关系如图所示。下列有关叙述正确的是

A. 随溶液pH增大,c(CO32-)/c(HCO3-)的值先减小后增大
B. 25℃时,碳酸的第一步电离常数Ka1=10-6
C. pH=4 的溶液中:c(H2CO3)+ c(HCO3-)+ c(CO32-)=0.1mol/L
D. b点所示的溶液中:c(Na+)+c(H+)= 2c(CO32-)+c(OH-)+c(Cl-)
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源: 题型:
【题目】如表是A、B、C、D、E五种有机物的有关信息:
A | ①能使溴的四氯化碳溶液褪色 ②比例模型为 ③能与水在一定条件下反应生成C |
B | ①由C、H两种元素组成 ②球棍模型为 |
C | ①由C、H、O三种元素组成 ②能与Na反应 ③与E反应生成相对分子质量为88的酯 |
D | ①相对分子质量比C少2 ②能由C催化氧化得到 |
E | ①由C、H、O三种元素组成 ②其水溶液能使紫色石蕊溶液变红 ③可由C发生氧化反应得到 |
回答下列问题:
(1)A~E中,属于烃的是________(填字母)。
(2)A能使溴的四氯化碳溶液褪色,发生反应的化学方程式为_______。
(3)C催化氧化生成D的化学方程式为_____________________。
(4)有机物B具有的性质是________(填序号)。
①无色无味的溶液;②有毒;③不溶于水;④密度比水大;⑤能使酸性KMnO4溶液和溴水褪色
(5)写出B与溴在催化剂作用下发生反应的化学方程式为_______。
(6)写出E与C反应生成相对分子质量为88的酯的化学方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.1mol·L-1CH3COOH溶液中存在如下电离平衡:CH3COOH![]() CH3COO-+H+对于该平衡,下列叙述正确的是 ( )
CH3COO-+H+对于该平衡,下列叙述正确的是 ( )
A. 加入水时,平衡向逆反应方向移动
B. 加入少量NaOH固体,平衡向正反应方向移动
C. 加入少量0.1mol·L-1HCl溶液,溶液中c(H+)减小
D. 加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常状况下,下列物质中①硫酸钡 ②醋酸 ③氯化氢 ④三氧化硫 ⑤氯气 ⑥碳酸钠 ⑦铜 ⑧硫酸溶液 ⑨氢氧化钾 ⑩乙醇(下列各空填序号)
(1)属于强电解质的是:________________。
(2)属于弱电解质的是:________________。
(3)能导电的是:________________。
(4)属于非电解质的是:________________。
(5)碳酸钠溶液显碱性的原因________(用离子方程式表达)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸是重要的化工材料,二氧化硫生成三氧化硫是工业制硫酸的重要反应之一。
(1)将0.050 mol SO2和0.030 mol O2放入容积为1 L的密闭容器中,反应2SO2(g)+O2(g)![]() 2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040 mol/L。
2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040 mol/L。
①从平衡角度分析采用过量O2的目的是________________________;
②计算该条件下反应的平衡常数K=________________________。
③已知:K(300℃)>K(350℃),该反应是________热反应。若反应温度升高,SO2的转化率________ (填“增大”、“减小”或“不变”)。
(2)某温度下,SO2的平衡转化率(![]() )与体系总压强(P)的关系如图1所示。平衡状态由A变到B时,平衡常数K(A)_____K(B)(填“>”、“<”或“=”,下同)。
)与体系总压强(P)的关系如图1所示。平衡状态由A变到B时,平衡常数K(A)_____K(B)(填“>”、“<”或“=”,下同)。
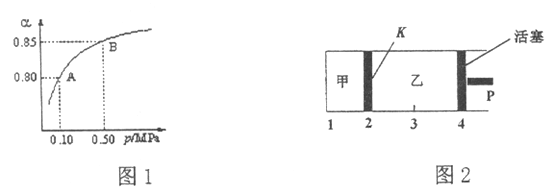
(3)如图2所示,保持温度不变,将2 mol SO2和1 mol O2加入甲容器中,将4 mol SO3加入乙容器中,隔板K不能移动。此时控制活塞P,使乙的容积为甲的2倍。
①若移动活塞P,使乙的容积和甲相等,达到新平衡时,SO3的体积分数甲______乙。
②若保持乙中压强不变,向甲、乙容器中通入等质量的氦气,达到新平衡时,SO3的体积分数甲_______乙。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是一门以实验为基础的自然科学,用下列各装置或其组合能完成相应实验的是(已知实验室可用块状硫化亚铁(FeS)与稀硫酸反应制取硫化氢(H2S)气体)

A. 装置②⑦可用于制取并收集干燥的CO2
B. 装置①⑤可用于制取并收集氧气
C. 装置②⑥可用于制取并收集硫化氢(H2S)气体
D. 装置④装满水后可以收集并储存氧气,需要氧气时可用水将装置中的氧气排出,水应从b端通入
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是以有机物A合成聚酯类高分子化合物F的路线:

已知:
回答下列问题:
(1)A生成B的反应类型为_____,C中的官能团名称为________。
(2)D与NaOH水溶液反应的化学方程式为________。
(3)①E生成F的化学方程式为________。
②若F的平均相对分子质量为20000,则其平均聚合度为________。(填字母)
A.54 B.108 C.119 D.133
(4)E在一定条件下还可以合成含有六元环状结构的G。G的结构简式为________。
(5)满足下列条件的C的同分异构体有_____种。(不考虑立体异构)
①含有1个六元碳环且环上相邻4个碳原子上各连有一个取代基
②1mol该物质与斐林试剂反应产生2mol砖红色沉淀
(6)写出用![]() 为原料制各化合物
为原料制各化合物 的合成路线______。(其他试剂任选)
的合成路线______。(其他试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】归纳总结是学习化学的一种方法。
(1)甲同学发现A、B、C三种物质有如图l所示的相互反应关系,“—”表示能反应(部分反应物、生成物以及反应条件省略,下同)。

已知A是常见金属,人体缺乏A元素易患贫血症;B是胃酸的主要成分;B与C反应产生不溶于稀硝酸的白色沉淀,则A是____(填化学式,下同),C是_______。请写出下列反应的化学方程式:A与B________________;B与C____________________。
(2)乙同学发现X、Y、Z三种物质有如图2所示的循环转化关系“→”表示能转化。
①若X、Y、Z均为含钙化合物,X是一种常用干燥剂,Y俗称熟石灰。则X的化学式为______;请写出Y→Z的反应化学方程式________________。
②若X是碳单质,Y、Z是含有碳元素的氧化物,X、Y、Z的相对分子质量依次增大,则Y的相对分子质量为___;Z→X可通过以下反应实现:___________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G为7种短周期主族元素,其原子序数依次增大。A、C可形成A2C和A2C2两种化合物,B的最高正化合价与最低负化合价的绝对值之差为2,D和A同主族,E是地壳中含量最高的金属元素,F和C同主族且可形成FC2和FC3两种化合物。
(1)G的元素名称是__________,它在元素周期表中的位置是______________。
(2)F的质子数和中子数相等,F的原子组成符号为______,它的最高价为____价。
(3)C、D可形成一种淡黄色固体化合物,写出此化合物的电子式__________。
(4)由上述7种元素中的4种元素组成的化合物X,X既能与热的NaOH溶液反应,也能与稀盐酸反应,且均能生成无色气体,X的化学式是____________________。
(5)已知Se在第四周期,与S同主族,请任意写出一种含Se物质的化学式,预测其性质,并说明预测依据_______。
含Se物质化学式 | 性质 | 预测依据 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com