
| A、常温下,氨水与(NH4)2SO4溶液混合后pH=7的溶液中,c(NH4+):c(SO42-) |
| B、相同温度下,1 mol.L-1醋酸与0.5mol.L-1醋酸中c(H+)之比 |
| C、用同浓度盐酸中和相同体积pH均为12的Ba(OH)2和KOH,所需盐酸的体积之比 |
| D、pH=2的H2SO4溶液与pH=2的CH3COOH溶液中,c(CH3COOH):c(H2SO4) |


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 丁 |
| 丁 |
| 甲 |
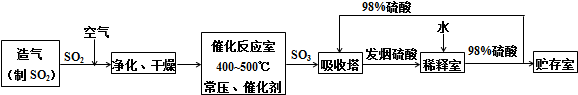
| A、若甲为焦炭,则丁可能是O2 |
| B、若甲为SO2,则丁可能是氨水 |
| C、若甲为NaAlO2溶液,则丁可能是盐酸 |
| D、若甲为CuCl2,则丁可能是氨水. |
查看答案和解析>>
科目:高中化学 来源: 题型:
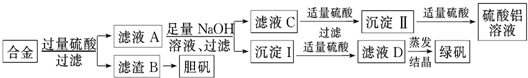
| A、x等于6 |
| B、性质稳定,不易脱色 |
| C、易溶于强酸和强碱 |
| D、可用氧化物形式表示BaO?CuO?2SiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
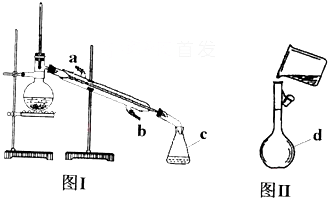
| A、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的底部 |
| C、萃取操作时,应选择有机萃取剂,且萃取剂的密度必须必水大 |
| D、蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学式 | 电离常数 |
| HClO | Ka=3×10-8 |
| H2CO3 | Ka1=4.3×10-7 |
| Ka2=5.6×10-11 | |
| CH3COOH | Ka=1.8×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、已知稀盐酸和稀NaOH溶液反应生成1molH2O时放出57.3kJ的热量,则稀硫酸和氢氧化钡溶液反应生成1molH2O时也放出57.3kJ的热量 | ||
B、C(石墨)+
| ||
| C、同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 | ||
| D、已知:①S(g)+O2(g)=SO2(g)△H=akJ.mol-1②S(s)+O2(g)=SO2(g)△H=bkJ.mol-1,则a<b |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com