
 镍(Ni)是一种重要的金属,金属镍及其化合物在合金材料以及催化剂等方面应用广泛.
镍(Ni)是一种重要的金属,金属镍及其化合物在合金材料以及催化剂等方面应用广泛.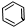 、④HCHO其中碳原子采取sp2杂化的分子有①③④(填物质序号),HCHO分子的立体结构为平面三角形;
、④HCHO其中碳原子采取sp2杂化的分子有①③④(填物质序号),HCHO分子的立体结构为平面三角形;分析 (1)Ni是28号元素,根据能量最低原则、泡利不相容原理和洪特规则,写出其核外电子排布式为:1s22s22p43s23p43d84s2,据此判断其外围电子排布式;
(2)根据碳原子含有的σ键和孤电子对判断碳原子采取的杂化方式; 根据价层电子对互斥理论判断甲醛的空间构型;
(3)离子晶体的熔点与离子键的强弱有关,离子所带电荷数越多,离子半径越小,离子键越强,熔点越高;
(4)因为Ni0、Fe0的晶体结构类型均与氯化钠的相同,而氯化钠中阴阳离子的配位数均为6,所以Ni0晶胞中Ni和O的配位数也均为6;
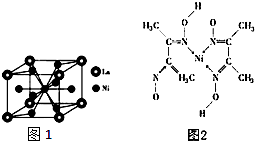
(5)晶胞中镧原子数8×$\frac{1}{8}$=1;镍原子数=1+8×$\frac{1}{2}$=5,由此可判断出化学式;
(6)碳氮之间是双键,双键是由一个σ键和一个π键构成;镍原子有空轨道,氮原子有孤电子对,因此二者形成配位键;丁二酮肟中甲基中的碳原子都是单键,在与氮相连的碳上有碳氮双键,据此判断杂化方式.
解答 解:(1)Ni是28号元素,其核外电子排布式为:1s22s22p43s23p43d84s2,价电子数为10,价电子排布式为3d84s2,
故答案为:3d84s2;
(2)①CH2=CH2中每个碳原子含有3个σ键,不含孤电子对,所以采取sp2杂化;
②HC≡CH中每个碳原子含有2个σ键,不含孤电子对,所以采取sp杂化;
③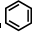 中每个碳原子含有3个σ键,不含孤电子对,所以采取sp2杂化;
中每个碳原子含有3个σ键,不含孤电子对,所以采取sp2杂化;
④HCHO中碳原子含有3个σ键,不含孤电子对,所以采取sp2杂化;
故碳原子采取sp2杂化的分子有①③④;
HCHO中碳原子含有3个σ键,不含孤电子对,所以其空间构型是平面三角形;
故答案为:①③④; 平面三角;
(3)Ni0、Fe0的晶体结构类型均与氯化钠的相同,说明二者都是离子晶体,离子晶体的熔点与离子键的强弱有关,离子所带电荷数越多,离子半径越小,离子键越强,熔点越高.由于Ni2+的离子半径小于Fe2+的离子半径,属于熔点是NiO>FeO,
故答案为:>;
(4)因为Ni0、Fe0的晶体结构类型均与氯化钠的相同,而氯化钠中阴阳离子的配位数均为6,所以Ni0晶胞中Ni和O的配位数也均为6.故答案为:6;6;
(5)晶胞中镧原子数8×$\frac{1}{8}$=1;镍原子数=1+8×$\frac{1}{2}$=5,所以化学式为LaNi5,故答案为:LaNi5;
(6)①碳氮之间是双键,双键是由一个σ键和一个π键构成;镍原子有空轨道,氮原子有孤电子对,因此二者形成配位键;
②氧原子与氢原子之间可以形成氢键;
③丁二酮肟中甲基中的碳原子都是单键,在与氮相连的碳上有碳氮双键,因此杂化类型是sp2和sp3杂化,
故答案为:①一个σ键、一个π键;配位键;②氢键;③sp2、sp3.
点评 本题考查晶体的结构与物质的性质的相互关系及应用,做题时注意电子排布式的书写方法,晶体熔点比较发放,分子空间构型的判断方法以及晶胞的有关计算,注意学习中有关做题方法的积累.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 将0.1mol的镁、铝混合物溶于100mL 4mol/LHCl溶液中,然后再滴加1mol/L NaOH溶液.请回答:
将0.1mol的镁、铝混合物溶于100mL 4mol/LHCl溶液中,然后再滴加1mol/L NaOH溶液.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 96倍 | B. | 48倍 | C. | 12倍 | D. | 32倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
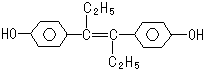
| A. | 遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物 | |
| B. | 1mol该有机物可以与5mol Br2发生反应 | |
| C. | 可分别与NaOH和NaHCO3发生反应 | |
| D. | 该有机物分子中,所有原子可能共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,X分子的空间构型为三角锥形.
,X分子的空间构型为三角锥形.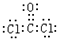 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
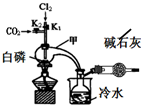 三氯化磷(PCl3)是合成药物的重要化工原料,可通过白磷和氯气化合得到.
三氯化磷(PCl3)是合成药物的重要化工原料,可通过白磷和氯气化合得到.| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 |
| 白磷 | 44.1 | 280.5 | 1.82 |
| PCl3 | -112 | 75.5 | 1.574 |
| POCl3 | 2 | 105.3 | 1.675 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某同学通过如下实验,探究化学反应中的能量变化.
某同学通过如下实验,探究化学反应中的能量变化. ,用湿润的红色石蕊试纸检验该气体.
,用湿润的红色石蕊试纸检验该气体.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com