


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2010�������ĵ����һ�и߶���ѧ�����п��Ի�ѧ�Ծ� ���ͣ�ʵ����
��.�����й�ʵ�����������˵������ȷ���� ������ĸ��
| A���ζ�ʱ���۾�Ӧʼ��ע�ӵζ�����Һ��ı仯 |
| B���ü�ʽ�ζ�����ȡ0.10 mol��L��1��KMnO4��Һ15.10 mL |
| C������к͵ζ�֮ǰ����ƿ������ˮϴ�����ɣ������ô���Һ��ϴ |
| D����pH��ֽ����ij��Һ��pHʱҪ�Ƚ���ֽ��ʪ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�츣��ʡ��һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й�ʵ��ԭ���������ȷ���� (���� )
A������һ�����ʵ���Ũ��ϡ����ʱ����ȡһ�������Ũ����ע���ձ�����ˮϡ����ȴ��ת�Ƶ�����ƿ��
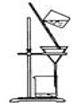
B��ϴ�ӳ���ʱ������ͼ������©���м�����ˮ�����貢�˸�
C���ø����pH��ֽ�ɲ��������ˮ��pH="2"
D������FeSO4��Һʱ����������Һ�м����������ۣ�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ��һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ʵ����
��16�֣���һ�������й�ʵ��������жϲ���ȷ���� ������ţ���ѡ�۷֣���
A������һ�����ʵ���Ũ����Һ������ʱƽ�ӿ̶��ߡ�
B���������Ȼ�̼���Ҵ������л��ܼ�����������ȡ��ˮ�е��塣
C����һ����ͨ�����壬�Ӵ�ֱ�ڹ��ߵķ�����Կ���һ�������ġ�ͨ·����
D������100mL 1mol/L ��NaOH��Һ�������4g ���������ƹ��塣
E���ò�˿պȡ������Һ����ɫ��Ӧ,û�й۲쵽��ɫ,���Ը���Һ�в�����Ԫ��
������ʵ������Ҫ480mL0.1mol/LNa2CO3��Һ������̼���ƾ������ƣ��ش���������
(1)Ӧ��������ƽ��ȡʮˮ��̼���ƣ�Na2CO3��10H2O������ g��
(2)���ڳ�����Ʒʱ,ҩƷ������ƽ������,���������ƽ�����ϣ�1g���������룬��ƽƽ��ʱ,��ʵ�ʳ�����ʮˮ��̼�������� (��ƫ�ߡ�ƫ�͡�����)��
(3) Na2CO3�� �� ��
(4) ��ʵ�����������,��Һ��Ũ�Ƚ��ᣨ��ƫ�� ��ƫ�� ������)
A����ˮ����ʱ���ӿ̶���
B������ƿ�ڱڸ���ˮ���δ���ﴦ��
C���ߵ�ҡ�Ⱥ��ְ�Һ����ڿ̶����ּ�ˮ����
D��������̼���ƾ��岿��ʧ�ᾧˮ
(5)�������Ǽ�ˮ�����˿̶��ߣ���ȷ�Ĵ���������
(6)��������ѱ�ǩ�ϵ�����дһ��(����ͼ)��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010�������ĵ����һ�и߶���ѧ�����п��Ի�ѧ�Ծ� ���ͣ�ʵ����
��.�����й�ʵ�����������˵������ȷ���� ������ĸ��
A���ζ�ʱ���۾�Ӧʼ��ע�ӵζ�����Һ��ı仯
B���ü�ʽ�ζ�����ȡ0.10 mol��L��1��KMnO4��Һ15.10 mL
C������к͵ζ�֮ǰ����ƿ������ˮϴ�����ɣ������ô���Һ��ϴ
D����pH��ֽ����ij��Һ��pHʱҪ�Ƚ���ֽ��ʪ
E���ζ��ܾ�����ˮϴ����ֱ��ע���Һ����ʹ��õĴ���ҺŨ��ƫ��
F���ù㷺pH��ֽ����H2SO4��Һ��pHʱ�����pH=3.2
G���ⶨ���ζ����ߣ���ʼʱ���Ժͼ�¼�ļ������СЩ���ζ����յ㸽����Ҫ��Щ
��.��1����������������Ӧ����1 molˮ��������241.8kJ��д���÷�Ӧ���Ȼ�ѧ����ʽ ����֪H2O(l) �� H2O(g) ��H ����44 kJ��mol��1 ���״����33.6 L H2 ����Һ̬ˮʱ�ų��������� kJ��
��2����ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̡���ѧ���ļ������γɣ����1mol��ѧ��ʱ�ͷţ������գ�����������֪����P4��P4O6�ķ��ӽṹ����ͼ��ʾ��
���ṩ���»�ѧ���ļ��ܣ�P-P 198 kJ��mol��1 P-O 360 kJ��mol��1,������������ԭ�Ӽ�ģ�O=O������Ϊ498 kJ��mol��1����P4+3O2 = P4O6�ķ�Ӧ�Ȧ�HΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010���������ʮ���и߶���ѧ�����п��Ի�ѧ�� ���ͣ������
��.�����й�ʵ������У���������_____������ţ���
A.��������ƽ��ȡ11.70 gʳ��
B.����Ͳ��ȡ12.36 mL����
C.����ʽ�ζ�����ȡ21.20 mL 0.10 mol/L H2SO4��Һ
D.��200 mL����ƿ����500 mL 0.1 mol/L NaCl��Һ
E.�ⶨ��Һ��pHʱ���ýྻ������IJ�����պȡ��Һ������������ˮ��ʪ����pH��ֽ�ϣ��������ɫ���Ƚ�
��.�������ʵ���Ũ��Ϊa mol/L�ı�����װ�ڵζ�����ȥ�ⶨV mL NaOH��Һ�����ʵ���Ũ�ȣ�����д���пհף�
��1����ʽ�ζ���������ˮϴ����Ӧ�ý��еIJ�����______ ____��
��2�����ڵζ�ǰ�ζ��ܼ��첿���������ݣ��ζ���ζ��ܼ��첿��������ʧ����ⶨ��NaOH���ʵ���Ũ�ȣߣߣ�ѡ�ƫ����ƫС������Ӱ�족��
������п��ʯī���������ϡ�������������ͭ��ɵĻ����Һ���������Һ���γɵ�ԭ����У������Ϸ����ķ�Ӧ�ĵ缫��Ӧʽ�ǣ� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com