
| A. | 原混合溶液中c(K+)为4mol/L | |
| B. | 原溶液中c(Cu2+)为1mol/L | |
| C. | 电解后溶液中c(H+)为8mol/L | |
| D. | 电解后加入1molCu(OH)2可使溶液复原 |
分析 KNO3和Cu(NO3)2的混合溶液进行电解,根据两极上的放电顺序确定放电的离子,阳极上的电极反应式:4OH-→2H2O+O2↑+4e-,当产生22.4L即1mol(标准状况)氧气时,转移电子是4mol,阴极上先发生电极反应:Cu2++2e-→Cu,然后是:2H++2e-→H2↑,在阴极上生成1mol的氢气时,转移电子是2mol,所以铜离子共得到电子是2mol,根据电子守恒结合两极均收到22.4L气体(标准状况)进行计算.
解答 解:KNO3和Cu(NO3)2的混合溶液中,阳极上的电极反应式:4OH-→2H2O+O2↑+4e-,当产生22.4L即1mol(标准状况)氧气时,转移电子是4mol,阴极上先发生电极反应:Cu2++2e-→Cu,然后是:2H++2e-→H2↑,在阴极上生成1mol的氢气时,转移电子是2mol,所以铜离子共得到电子是2mol,所以铜离子的物质的量为1mol,所以c(Cu2+)=2mol/L.
A、根据c(Cu2+)=2mol/L,所以Cu(NO3)2的浓度是2mol/L,其中的c(NO3-)=4.0mol/L,但是总共的c(NO3-)=6.0mol/L,所以原混合溶液中硝酸钾的浓度是2mol/L,所以c(K+)为2mol/L,故A错误;
B、KNO3和Cu(NO3)2的混合溶液中,阳极上的电极反应式:4OH-→2H2O+O2↑+4e-,当产生22.4L即1mol(标准状况)氧气时,转移电子是4mol,阴极上先发生电极反应:Cu2++2e-→Cu,然后是:2H++2e-→H2↑,在阴极上生成1mol的氢气时,转移电子是2mol,所以铜离子共得到电子是2mol,所以铜离子的物质的量为1mol,所以c(Cu2+)=2mol/L,故B错误;
C、阳极上的电极反应式:4OH-→2H2O+O2↑+4e-,当产生22.4L即1mol(标准状况)氧气时,转移电子是4mol,消耗了氢氧根离子是4mol,阴极上发生了电极反应2H++2e-→H2↑,在阴极上生成1mol的氢气时,转移电子是2mol,消耗的氢离子是2mol,所以相当于溶液中含有2mol的氢离子,所以电解后溶液中,如果是忽略体积变化,则c(H+)=$\frac{2mol}{0.5L}$=4mol/L,但是体积是变化的,故C错误;
D、根据电解原理:出什么加什么,阳极上的电极反应式:4OH-→2H2O+O2↑+4e-,产生22.4L即1mol(标准状况)氧气,阴极上先发生电极反应:Cu2++2e-→Cu,然后是:2H++2e-→H2↑,在阴极上生成1mol的氢气时,转移电子是2mol,所以铜离子共得到电子是2mol,所以铜离子的物质的量为1mol,产生氢气1mol、氧气1mol和金属铜1mol,所以电解后加入1molCu(OH)2可使溶液复原,故D正确.
故选D.
点评 本题考查电解池的工作原理知识,注意离子的放电顺序在解题中的应用以及电子守恒的思想的应用,属于综合知识的考查,难度不大.


科目:高中化学 来源: 题型:选择题

| A. | 用装置①分离碘并回收苯 | |
| B. | 用装置②灼烧海带灰 | |
| C. | 用装置③配置一定物质的量浓度的H2SO4溶液 | |
| D. | 用装置④蒸发浓缩MgCl2溶液制取MgCl2•6H2O晶体 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学卷(解析版) 题型:选择题
常温下,10mL浓度为amol·L-1的醋酸溶液pH=4。下列能使溶液的pH=7的措施是
A.将溶液稀释到 10L
B.将溶液与10mL浓度为amol·L-1的NaOH溶液混合
C.将溶液与10mL、pH=10的NaOH溶液混合
D.往溶液中加入适量的氢氧化钠,使溶液中c(Na+)=c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学卷(解析版) 题型:选择题
对于化学反应3W(g)+2X(g)=4Y(g)+3Z(g),下列反应速率关系中,正确的是
A.υ(W)=3υ(Z) B.2υ(X)=3υ(Z) C.2υ(X)=υ(Y) D.3υ(W)=2υ(X)
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2O3(Al2O3)用盐酸 | B. | Fe2O3(Al2O3)用氨水 | ||
| C. | Mg(Al)用纯碱溶液 | D. | MgCl2(AlCl3)用氢氧化钠溶液和盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | Cu2+ | H+ | Cl- | SO42- |
| c/mol•L-1 | 1 | 4 | 4 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
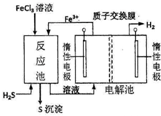 现代工业生产中常用电解氯化亚铁的方法制得氯化铁溶液吸收有毒的硫化氢气体.工艺原理如图所示.下列说法中不正确的是( )
现代工业生产中常用电解氯化亚铁的方法制得氯化铁溶液吸收有毒的硫化氢气体.工艺原理如图所示.下列说法中不正确的是( )| A. | 左槽中发生的反应是:2Cl--2e-═Cl2↑ | |
| B. | 右槽中的反应式:2H++2 e-═H2↑ | |
| C. | H+从电解池左槽迁移到右槽 | |
| D. | FeCl3溶液可以循环利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
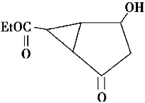 及其核磁共振氢谱图如下:下列关于该有机物的叙述正确的是( )
及其核磁共振氢谱图如下:下列关于该有机物的叙述正确的是( )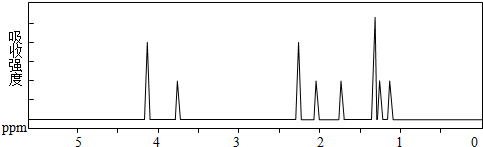
| A. | 该有机物不同化学环境的氢原子有6种 | |
| B. | 该有机物属于芳香族化合物 | |
| C. | 键线式中的Et代表的基团为-CH3 | |
| D. | 该有机物的分子式为C9H12O4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com