
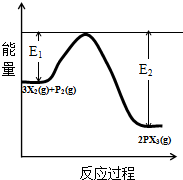
分析 (1)①△H1=Ea正-Ea逆>0,所以Ea正>△H1;温度的改变对吸热反应方向影响较大,由此分析解答;
(2)达平衡状态时各组分的浓度保持不变,正逆反应速率相等,由此分析解答.
解答 解:(1)①△H1=Ea正-Ea逆>0,所以Ea正>△H1;温度的改变对吸热反应方向影响较大,所以对正反应方向影响较大,故答案为:大于;正;
(2)A.两边气体的计量数相等,混合气的平均相对分子质量始终不随时间而变化,故错误;
B.当v(CO)正=v(H2)逆=v(CO)逆,正逆反应速率相等,故正确;
C.当c(CO2)•c(H2)=c(CO)•c(H2O)时,并不是浓度不变的状态,故C错误;
D.两边气体的计量数相等,混合气的压强一直不随时间而变化,故错误;
故选B.
点评 本题考查化学平衡状态的判断,题目难度不大,应注意根据平衡状态的特点分析.


科目:高中化学 来源: 题型:选择题
| A. | 甲烷分子的球棍模型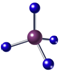 | |
| B. | Cl-的结构示意图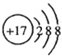 | |
| C. | 中子数为8的碳原子的核素符号为12C | |
| D. | 中子数为1的氢原子的核素符号为21H |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| X | Y | Z | W | R | P | Q | |
| 原子半径/nm | 0.154 | 0.074 | 0.099 | 0.075 | 0.143 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | -3,+5 | +3 | ||
| 其他 | 阳离子核外无电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al$\stackrel{氧气,加热}{→}$Al2O3$\stackrel{硝酸}{→}$Al(NO3)3$\stackrel{加热蒸干}{→}$硝酸铝晶体 | |
| B. | Cu$\stackrel{氧气,加热}{→}$CuO$\stackrel{稀硫酸}{→}$CuSO4$\stackrel{蒸干结晶}{→}$胆矾 | |
| C. | Fe$\stackrel{氯气}{→}$FeCl3$\stackrel{过量氨水}{→}$Fe(OH)3$\stackrel{加热}{→}$Fe2O3 | |
| D. | FeSO4溶液$\stackrel{硫化氢、过滤}{→}$FeS |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
| 次数 | 第1次 | 第2次 |
| 加入稀盐酸的质量/g | 50 | 50 |
| 剩余固体的质量/g | 2.6 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (c-a-b)kJ | B. | (a+b-c)kJ | C. | (2c-a-b)kJ | D. | $\frac{2c-a-b}{2}$kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com