
已知温度T时水的离子积常数为KW,该温度下,将浓度为a mol· L-1的一元酸HA与b mol· L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是 ( )
A.a=b
B.混合溶液的pH=7
C.混合溶液中,[H+]= mol·L·-1
mol·L·-1
D.混合溶液中,c(H+)+c(B+)===c(OH-)+c(A-)
科目:高中化学 来源: 题型:
“绿色化学实验”已走进课堂,下列做法符合“绿色化学”的是( )
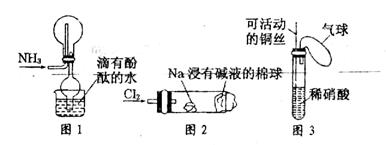
①实验室收集氨气采用图1所示装置
②实验室中做氯气与钠的反应实验时采用图2所示装置
③实验室中用玻璃棒分别蘸取浓盐酸和浓氨水做氨气与酸生成铵盐的实验
④实验室中采用图3所示装置进行铜和稀硝酸的反应
A.②③④ B.①②③ C.①②④ D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
工业制备氯化铜时,将浓盐酸用蒸气加热到80℃左右,慢慢加入粗CuO粉末(含杂质Fe2O3、FeO),充分搅拌使之溶解,得一强酸性的混合溶液,现欲从该混合溶液中制备纯净的CuCl2溶液[参考数据:pH≥9.6时,Fe2+完全水解成Fe(OH)2;pH≥6.4时,Cu2+完全水解成Cu(OH)2;pH≥3.7时,Fe3+完全水解成Fe(OH)3]。请回答以下问题:
(1)第一步除Fe2+,能否直接调整pH=9.6将Fe2+沉淀除去?______,理由是______
_____________________________________________________________________。
有人用强氧化剂NaClO将Fe2+氧化为Fe3+:
①加入NaClO后,溶液的pH变化是___________(填序号);
A.一定增大 B.一定减小
C.可能增大 D.可能减小
②你认为用NaClO作氧化剂是否妥当?__________,理由是_________________
___________________________________________________________。
③现有下列几种常用的氧化剂,可用于除去该混合溶液中Fe2+的有_________(填序号)。
A.浓HNO3 B.KMnO4 C.Cl2 D.O2
(2)除去溶液中的Fe3+的方法是调整溶液的pH=3.7,现有下列试剂均可以使强酸性溶液的pH调整到3.7,可选用的有__________(填序号)。
A.NaOH B.氨水 C.Cu2(OH)2CO3 D.Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
已知常温下,浓度均为0.1 mol·L-1的4种钠盐溶液pH如下表:
| 溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 5.2 |
下列说法中正确的是
A.足量SO2通入NaClO溶液中发生反应的离子方程式为:H2O+SO2+ClO-=HClO+HSO3-
B.向氯水中加入NaHCO3,可以增大氯水中次氯酸的浓度
C.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO溶液,pH最大的是H2SO3
D.NaHSO3溶液中离子浓度大小顺序为:c(Na+)> c(H+)>c(HSO3-) >c(SO32-)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A.食盐溶液中除去SO 最合适的试剂是Ba(NO3)2
最合适的试剂是Ba(NO3)2
B.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同
C.25 ℃时,用醋酸溶液中和等浓度NaOH溶液至pH=7,VCH3COOH<VNaOH
D.AgCl易转化为AgI沉淀且Ksp(AgX)=[Ag+]·[X-],故Ksp(AgI)<Ksp(AgCl)
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,将某一元酸HA和NaOH溶液等体积混合,实验信息如下:
| 实验编号 | c(HA)/ mol·L-1 | c(NaOH)/ mol·L-1 | 反应后溶液pH |
| 甲 | 0.1 | 0.1 | pH=9 |
| 乙 | c1 | 0.2 | pH=7 |
下列判断不正确的是 ( )
A.c1一定大于0.2 mol·L-1
B.HA的电离方程式是HA H++A-
H++A-
C.甲反应后溶液中:c(Na+) > c(OH-) > c(A-) > c(H+)
D.乙反应后溶液中:c(Na+) < c(HA)+c(A-)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-)
B.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.c(Cl-)>c(H+)>c(NH4+)>c(OH-)
D.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
(1)若溶液中只溶解了一种溶质,该溶质是 ,上述离子浓度大小顺序关系中正确的是(选填序号) 。
(2)若上述关系中D是正确的,混合后溶液中的溶质为 。
(3)25 ℃时,将a mol·L-1的氨水与b mol·L-1盐酸等体积混合,反应后溶液恰好显中性,则混合前a b(填“>”、“<”、或“=”), 用a、b表示NH3·H2O的电离平衡常数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液一定呈中性的是
A.将pH=5的盐酸稀释100倍所得溶液
B. c(H+)=1.0×10-7mol/L
C.c(H+)=c(OH-)=1×10-6mol/L的溶液
D.非电解质溶于水得到的溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com