
| T/K | 303 | 313 | 323 | 353 |
| NH3生成量/(10-6 mol) | 4.8 | 5.9 | 6.0 | 2.0 |
 N2(g)+3H2O(l) 2NH3(g)+
N2(g)+3H2O(l) 2NH3(g)+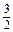 O2(g)
O2(g)






 (3)工业合成氨的反应为N2(g)+3H2(g) 2NH3(g)。设在容积为2.0 L的密闭容器中充入
(3)工业合成氨的反应为N2(g)+3H2(g) 2NH3(g)。设在容积为2.0 L的密闭容器中充入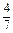 。计算:
。计算: ②该条件下反应2NH3(g) N2(g)+3H2(g)的平衡常数。
②该条件下反应2NH3(g) N2(g)+3H2(g)的平衡常数。

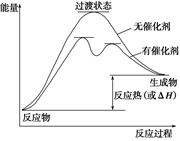







 N2(g)+3H2(g) 2NH3(g)
N2(g)+3H2(g) 2NH3(g)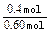 ×100%=66.7%
×100%=66.7% ②设反应2NH3(g) N2(g)+3H2(g)的平衡常数为K。平衡时,c(NH3)=2×0.40 mol÷2.0 L=
②设反应2NH3(g) N2(g)+3H2(g)的平衡常数为K。平衡时,c(NH3)=2×0.40 mol÷2.0 L=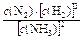 =[(0.10 mol·L-1?)×(0.20 mol·L-1)3]÷(0.40 mol·L-1)2
=[(0.10 mol·L-1?)×(0.20 mol·L-1)3]÷(0.40 mol·L-1)2

科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NH4H是离子化合物 | B.NH4H溶于水,所形成的溶液显酸性 |
| C.NH4H与水反应时,NH4H是氧化剂 | |
| D.NH4H固体投入少量的水中,有两种气体生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NO是一种红棕色的气体 | B.常温常压下,NO不能与空气中氧气直接化合 |
| C.含等质量的氧元素的NO和CO的物质的量相等 | |
| D.NO易溶于水,不能用排水法收集 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| A.铂丝的温度高,接触氨水会使氨气大量逸出 | B.红热铂丝会与氨水反应,使铂丝腐蚀 |
| C.防止铂丝温度降低而不能起催化作用 | D.防止爆炸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
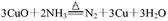
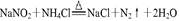
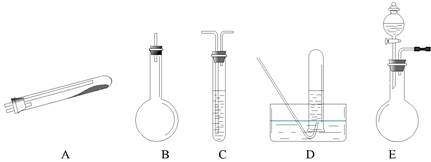
 ,最好要用上述仪器中 的(填仪器字母,下同)作为氨气发生装置。要制取并收集纯净的N2(允许含少量的水蒸气),还应使用到上述仪器中的
,最好要用上述仪器中 的(填仪器字母,下同)作为氨气发生装置。要制取并收集纯净的N2(允许含少量的水蒸气),还应使用到上述仪器中的 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com