
| A、合金的熔点一般比组分金属高 |
| B、合金中只含金属元素 |
| C、合金的机械性能一般比组分金属好 |
| D、合金不容易发生电化学腐蚀 |
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案科目:高中化学 来源: 题型:
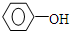 ;④CH3COOC2H5;⑤CH3COOH五物质中:
;④CH3COOC2H5;⑤CH3COOH五物质中:查看答案和解析>>
科目:高中化学 来源: 题型:
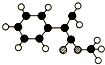 A是生产某新型工程塑料的基础原料之一,分子式为C10H10O2,其分子结构模型如图所示(如图中球与球之间连线代表化学键单键或双键).
A是生产某新型工程塑料的基础原料之一,分子式为C10H10O2,其分子结构模型如图所示(如图中球与球之间连线代表化学键单键或双键).查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KHCO3 KAlO2 K2CO3 KCl |
| B、K2CO3 KOH KHCO3 KCl |
| C、K2SO4 KOH KHSO4 KCl |
| D、K2CO3 K2SiO3 KOH KCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、α(A)=α(B) |
| B、α(A)>α′(A) |
| C、α(B)=α′(B) |
| D、α(A)=α′(A) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO32-、Na+、K+、OH- |
| B、Ba2+、CO32-、NO3-、SO42- |
| C、K+、Cu2+、Cl-、SO42- |
| D、Fe2+、NO3-、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com